作者简介:索明环,女,1982年生,硕士,主管技师,主要从事临床生化检验工作。
探讨在3种不同检测系统及不同的储存条件下全血糖化血红蛋白A1c(HbA1c)检测结果的稳定性差异。
方法选取3支用乙二胺四乙酸二钾(EDTA-K2)抗凝的不同HbA1c浓度的全血样本,分装后分别置常温(20~25 ℃)、4 ℃、-30 ℃、-70 ℃保存。分别于第1、3、5、7、14、21、28、35、42、56、84天用3种HbA1c检测系统[Bio-Rad variant ⅡTurbo HbA1c检测仪(阳离子离子交换高效液相色谱法),简称Bio-Rad variant ⅡTurbo;Primus Ultra2 HbA1c检测仪(亲和层析高效液相色谱法),简称Primus Ultra2;Roche Modular PPI全自动生化分析仪及配套试剂(免疫抑制比浊法),简称Roche Modular PPI]进行测定。
结果-70 ℃保存样本不同时间测定结果的差异较小,其中Bio-Rad variant ⅡTurbo测定样本的变异系数(
不同的检测系统及不同的样本存放条件HbA1c检测结果存在差异。
To investigate the stability differences of glycosylated hemoglobin A1c(HbA1c) measurement by 3 detection systems under different storage conditions.
MethodsThree whole blood samples anti-coagulated by ethylene diamine tetraacetic acid-K2(EDTA-K2) at 3 HbA1c levels were collected and stored at room temperature(20-25℃), 4℃,-30℃ and -70℃. One aliquot from each temperature was analyzed by each method on day 1, 3, 5, 7, 14, 21, 28, 35, 42, 56 and 84. The 3 detection systems were Bio-Rad variant Ⅱ Turbo HbA1c analyzer (positive ion exchange high performance liquid chromatography, Bio-Rad variant Ⅱ Turbo), Primus Ultra2 HbA1c analyzer (affinity high performance liquid chromatography, Primus Ultra2) and Roche Modular PPI automatic biochemistry analyzer and its reagents (inhibition immunoturbidimetry, Roche Modular PPI).
ResultsThe results of samples stored at -70℃ were similar at different days. The coefficient of variation (
The HbA1c measurement is differently detected by different systems under different storage conditions.
糖化血红蛋白A1c(glycosylated hemoglobin A1c,HbA1c)是糖尿病诊断和并发症控制的金标准。2010年美国糖尿病协会(American Diabetes Association, ADA)将HbA1c列为糖尿病诊断的标准[ 1]。HbA1c降低可以减少大血管及微血管病变,并且浓度的变化与患者的预后息息相关[ 2, 3]。保证HbA1c检测结果的准确性对临床诊断和监测糖尿病至关重要。在我国,某些医学实验室还没有开展这一项目的检测,且HbA1c的检测方法众多,标准化工作刚刚开展[ 4]。若要推广HbA1c的检测,保证标准化计划顺利实施就必须先了解样本储存及运送的条件,避免因为分析前因素导致结果的不可比。我们选用了目前医学实验室常规使用的3种HbA1c检测系统,通过对样本不同存放温度及时间的限制,了解样本的储存条件及稳定性,为医学实验室规范开展HbA1c检测和标准化计划及科学研究提供参考依据。
1. 阳离子离子交换高效液相色谱法(HPLC) 采用Bio-Rad variant ⅡTurbo 糖化血红蛋白检测仪(简称Bio-Rad variant ⅡTurbo)。应用配套的试剂、校准品、防护柱、分析柱及质控品。按厂家要求400个测试更换防护柱,2 000个测试更换分析柱,更换柱子后按要求进行活化定标。
2. 亲和层析HPLC 采用Primus Ultra2糖化血红蛋白检测仪(简称Primus Ultra2)及配套试剂、分析柱。校准品及质控品为Bio-Rad公司产品。按要求反转更换柱子,定期做酶清洗。
3. 免疫抑制比浊法 应用Roche Modular PPI全自动生化分析仪(简称Roche Modular PPI)及配套HbA1c测定试剂、校准品及质控品。
根据美国糖化血红蛋白标准化计划(National Glycohemoglobin Standardization Program,NGSP)储存校准品及质控品的稳定性标准,进行全血样本的稳定性评价。NGSP规定:HbA1c测定结果以-70 ℃或更低温度 ±3 s为可接受范围,在 ±3 s范围内结果稳定,否则为不稳定[ 5]。
1. 选取当日用Bio-Rad variant ⅡTurbo检测系统检测的分布范围为6.0%~7.0%、9.0%~10.0%及11.0%~12.0%的乙二胺四乙酸二钾(EDTA-K2)抗凝全血样本各5支,观察每支样本的检测结果分析图谱,摒弃存在异常图谱的样本。
2. 检测选取的全血样本的平均红细胞体积和平均红细胞血红蛋白浓度,同时用法国Sebia Capillary 2 毛细管电泳仪检测,排除地中海贫血和异常血红蛋白样本。
3. 最终选定3支样本,本实验室Bio-Rad variant ⅡTurbo检测结果分别为6.2%(样本1)、9.3%(样本2)、11.1%(样本3)。收集同一患者同一时间抽取的EDTA-K2抗凝血,混合后分装,每管50 μL。分别置于常温(20~25 ℃)、4 ℃、-30 ℃、-70 ℃保存,分别于第1、3、5、7、14、21、28、35、42、56、84天用3种检测系统检测,同一样本同一时间每个检测系统各检测2次,取平均值作为评价结果。
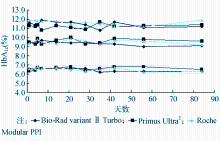
-70 ℃保存条件下3种检测系统的结果显示出很好的稳定性。其中Bio-Rad variant ⅡTurbo测定样本的变异系数( CV)为2.12%~2.80%;Primus Ultra2的 CV为2.19%~2.71%;Roche Modular PPI的 CV为2.28%~2.91%。Bio-Rad variant ⅡTurbo样本1结果的稳定性范围为5.97%~7.00%、样本2为8.78%~9.98%、样本3为10.48%~12.41%。Primus Ultra2样本1结果的稳定性范围为6.06%~7.14%、样本2为8.81%~10.41%、样本3为10.50%~11.97%。Roche Modular PPI样本1结果的稳定性范围为5.96%~7.10%、样本2为8.88%~10.20%,样本3为10.86%~12.45%。见图1、表1。
| 表1 -70 ℃保存样本3种检测系统测定结果的分析与比较(%) |
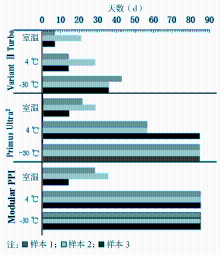
以表1所列的稳定性范围作为判断标准。当结果超出稳定性范围时,则稳定时间以上一次存储时间为准。当3个样本全部满足稳定性范围时,则判定该储存条件可保持样本稳定。3种检测系统检测样本的稳定性见表2和图2。
| 表2 3种检测系统HbA1c样本在不同条件下的稳定性 |
1. Bio-Rad variant ⅡTurbo 样本1常温条件下可稳定7 d、4 ℃可稳定14 d、-30 ℃可稳定35 d;样本2常温可稳定21 d、4 ℃可稳定28 d、-30 ℃可稳定35 d;样本3常温可稳定7 d、4 ℃可稳定14 d、-30 ℃可稳定42 d。因此,用Bio-Rad variant ⅡTurbo测定样本常温可稳定 7 d、4 ℃可稳定14 d、-30 ℃可稳定 35 d。
2. Primus Ultra2 样本1常温条件下可稳定14 d、4及-30 ℃均可稳定84 d;样本2常温可稳定21 d、4 ℃可稳定56 d、-30 ℃可稳定84 d;样本3常温可稳定14 d、4 ℃可稳定56 d,-30 ℃可稳定84 d。因此,用Primus Ultra2测定样本常温可稳定14 d、4 ℃可稳定56 d、-30 ℃可稳定84 d。
3. Roche Modular PPI 样本1常温条件下可稳定14 d、4及-30 ℃均可稳定84 d;样本2常温可稳定21 d、4及-30 ℃均可稳定84 d;样本3常温可稳定14 d,4及-30 ℃均可稳定84 d。因此,用Roche Modular PPI测定样本常温可稳定 14 d、4及-30 ℃均可稳定84 d。
HbA1c可反映机体2~3个月的血糖水平,不受患者当天抽血状态的影响,是评价糖尿病患者血糖控制状况极有价值的指标。美国ADA已经将其列为诊断糖尿病的标准。而国内还没有将HbA1c作为诊断标准,主要原因是国内检测HbA1c的方法众多,结果差异性较大。这2年国内加快了HbA1c的标准化进程。相信不久的将来,HbA1c也会成为中国糖尿病诊断的标准。但要保证HbA1c检测的正确性,就要对实验方法和检测系统的稳定性非常了解,本研究选用了3个常见的检测系统进行评价。
本研究选用的稳定性标准是用-70 ℃测定结果的均值的95%可信区间来判断。因为很多学者已经证明-70 ℃下存放的样本用离子交换HPLC测定至少1年是稳定的[ 6],并且-70 ℃保存样本也是DCCT参考实验室和NGSP网络实验室采用的保存质控品和校准品的条件[ 7, 8]。故采用此稳定性标准可靠、可行。
本研究中评价了3种不同方法、不同仪器、不同浓度样本、不同存放条件对检测结果的干扰,结果确实存在差异。Bio-Rad variant ⅡTurbo测定样本常温可稳定7 d,4℃可稳定14 d,-30 ℃可稳定35 d;而Little等[ 8]的结果显示Bio-Rad Variant Ⅱ为常温7 d、4 ℃ 57 d、-20 ℃ 28 d;并且王冬环等[ 9]检测结果也显示东曹G7测定的稳定性为-20℃ 14 d、4 ℃ 63 d。这3台仪器均采用离子交换HPLC,4 ℃稳定性相差较大,这也可能与仪器性能有关。因为Bio-Rad variant ⅡTurbo检测样本的速度与其他仪器比较提高了许多,但在一定程度上也牺牲了HPLC检测的稳定性;Primus Ultra2及Roche Modular PPI则显示出了较好的稳定性,与Little等[ 8]的检测结果[Primus CLC (385 and 330)显示全血稳定性为常温 14 d、4及-20 ℃ 57 d]一致。但在本研究中2种检测系统显示出了更好的稳定性,其中Primus Ultra2 4 ℃可稳定56 d、-30 ℃至少可稳定84 d,Roche Modular PPI 4及-30 ℃均至少可稳定84 d。这可能与不同的检测系统及检测方法有关。亲和层析HPLC是以糖基化位点的结构特异性为测定原理。HbA1c可以与亲和树脂连接,而非糖化血红蛋白不可以,因而被分离。亲和层析HPLC不受温度、氨基甲酰糖化血红蛋白和胎儿血红蛋白的干扰,结果可靠。免疫抑制比浊法是依据血红蛋白上糖化基团的结构特点而设计,原理是根据HbA1c与相应的单抗结合发生凝集反应的特性,受干扰因素也较小。因此,这2种检测系统显示出比较好的稳定性。
综上所述,不同的检测系统在不同的样本存放条件下,检测结果存在差异。实验室无论检测常规患者样本还是做实验研究,或实验标准化计划都应根据实验要求及检测系统做好样本的储存工作。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|