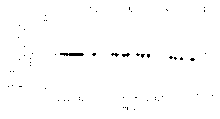作者简介:李俊华,女,1970年生,学士,主管技师,主要从事细胞学检验工作。
建立一种改良酶法尿素测定试剂,并评估其性能。
方法采用酶法测定尿素反应前后吸光度(
现有试剂空白
改良酶法尿素试剂具有更加优越的检测限和分析敏感性,并且自身性能良好,符合相关临床应用要求。
尿素是人体内氨基酸代谢的终产物,构成了血液中绝大部分的非蛋白氮,在肝脏内合成,经肾脏排泄到尿中,因此其含量取决于蛋白质的摄入、蛋白质分解代谢及肾功能[ 1]。尿素可自由地从肾小球滤出,因此是反映肾功能的敏感指标。本研究对现有酶法尿素检测试剂进行了改良,并对其性能指标进行了评估。
1.现有试剂
试剂1(R1):100 mmol/L 三羟甲基氨基甲烷缓冲液(pH值7.8),8 kU/L尿素酶,0.5 kU/L谷氨酸脱氢酶,1.5 mmol/L二磷酸腺苷,0.8 g/L叠氮钠;试剂2(R2):100 mmol/L三羟甲基氨基甲烷缓冲液(pH值9.6),0.3 mmol/L还原型β-烟酰胺腺嘌呤二核苷酸,13.0 mmol/L α-酮戊二酸,0.8 g/L叠氮钠。
2.改良试剂
R1:100 mmol/L三羟甲基氨基甲烷缓冲液(pH值9.1),0.3 mmol/L还原型β-烟酰胺腺嘌呤二核苷酸;R2:100 mmol/L三羟甲基氨基甲烷缓冲液(pH值7.6),40 kU/L尿素酶,2 kU/L谷氨酸脱氢酶,30 mmol/L α-酮戊二酸,0.8 g/L叠氮钠。
3.进口尿素试剂
进口和光尿素测定试剂(简称和光试剂)购自日本和光公司(批号TL953)。
4.校准品
改良试剂和现有试剂校准品均购自罗氏公司(批号169512-01)。和光试剂校准品为试剂盒自带。
5.仪器
日立7180全自动生化分析仪(日本日立公司)。
反应温度为37 ℃,比色杯光径为1.0 cm,检测主波长340 nm,副波长405 nm,样本(校准管以校准品做样本)加R1混匀,孵育3~5 min后加入R2混匀,孵育1.5 min后连续检测3 min吸光度( A)值变化。其中样本用量5 μL,R1用量200 μL,R2 用量50 μL,根据仪器使用说明及分析参数编制检测程序。现有试剂和改良试剂均采用罗氏校准品定标,和光试剂采用自带校准品定标。
有关试剂空白 A值及变化率、检测限、分析敏感性、精密度、线性范围、方法学比对和干扰试验等评价参照美国临床实验室标准化委员会EP系列文件及国内外惯用方法进行[ 2, 3, 4, 5]。
1.空白 A值及变化率
在波长340 nm(光径1.0 cm)处检测,以蒸馏水为样本,重复测定2次。
2.检测限
以蒸馏水为样本,用试剂重复测定20次。
3.分析敏感性
用3种试剂分别测定尿素浓度为16.7 mmol/L的样本,记录在试剂规定参数下产生的 A值改变,换算为 A值变化率。
4.精密度
按NCCLS EP5-A2文件[ 2]评价。取高值和低值的患者混合血清各1份,测定20次,评价批内精密度;取上述高、低值混合血清各自分装成20份,并于-20 ℃避光冰冻保存,每天取高、低值混合血清各1份,完全溶解后测定,计算批间精密度。
5.线性评价
按NCCLS EP6-A文件[ 3]评价。取尿素高、低值血清样本各1份。将高值和低值血清分别按不同比例混合稀释成不同浓度梯度的样本,并将这些样本随机排列进行测定,各个浓度重复测定5次,取其均值为测定值,与预期值做线性对比。
6.方法学比对试验
按NCCLS EP9-A2文件[ 4, 5]评价。每天收集检测范围均匀分布的8份患者新鲜血清,连续5 d,共40份样本。每份样本都用5种试剂各自进行双份测定,测定顺序依1→8测定第1次,再按反序8→1测定第2次,以减少交叉污染及漂移对重复测定标本平均值的影响,顺序中的浓度应尽可能随机排列。同一样本均在2 h内完成两法的测定。
7.干扰试验
按照NCCLS EP7-A文件[ 6]评价。分别测定加入干扰物的高、低值混合血清。
8.参考区间
按照NCCLS C28-A2文件[ 7]评价。采集240名健康参考个体血清样本进行检测。对正态分布的数据资料其参考区间由95%可信区间表示;对偏态分布的数据资料采用百分位数法表示。
所有数据用Excel 2007软件进行统计处理、作图分析及偏差评估计算。
现有试剂空白 A值为1.8,空白 A值变化率为-0.001 8;改良试剂空白 A值为1.8,空白 A值变化率为-0.001 9;和光试剂空白 A值为1.6,空白 A值变化率为-0.000 4。
现有试剂检测限为0.035 mmol/L,改良试剂检测限为0.014 mmol/L,和光试剂检测限为0.075 mmol/L。
现有试剂的分析敏感性为-0.04,改良试剂为-0.13,和光试剂为-0.05。
改良试剂测定高、低值血清的批内精密度分别为0.45%和0.85%,批间精密度分别为0.38%和0.71%。
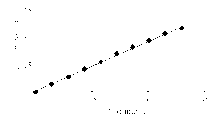
相关方程为 Y=0 .921 6 X+0 .595, R2=0.998 6。线性浓度范围为0~38 mmol/L。见图1:
注: Y= 0 .921 6 X + 0 .595; R2 = 0.998 6
1.检查离群点
通过计算可知试验评估系统(改良试剂)及参比系统(和光试剂)均无方法内和方法间离群点。
2.散点图、偏倚图分析
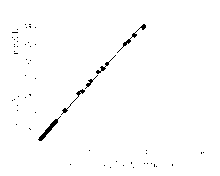
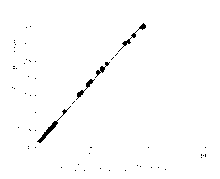
以和光试剂检测的测定结果为 X,改良试剂的检测结果为 Y,经组内、组间离群值检验后,画散点图和偏倚图。由散点图可知改良试剂与和光试剂之间的线性关系良好,见图2、图3:
注: Y= 0 .927 7 X + 0 .411 5; R2 = 0.999 1
注: Y= 0 .927 7 X + 0 .411 5; R2 = 0.999
由偏倚图可知改良试剂与和光试剂测定同一份血清时差值较小,分布较为合理,见图4、图5:
3. X值合适范围的检验及线性回归分析
对尿素测定结果进行相关回归分析, r=0.999>0.975,说明测定范围足够宽,误差的影响可以忽略不计。回归方程为 Y=0 .93 X+0.41。
4.偏差估计
根据NCCLS EP9-A2文件提供的公式[ 4],并选择尿素的2个医学决定水平14.2和28.0 mmol/L,对预期偏倚及可信区间进行计算,判断2种试剂是否相当。以美国临床实验室改进修正法规(CLIA'88)的允许误差(9%)为限,计算得其允许偏倚分别为1.28和2.52 mmol/L。2个医学决定水平的预期偏差95%可信区间上限均低于各自的允许偏倚,见表1:
| 表1 预期偏倚及可信区间的比较 |
说明改良试剂与和光试剂的偏倚可接受,试剂间检测结果具有良好的可比性。
以相对偏差≥10%作为有明显干扰的评判指标。342 μmol/L结合胆红素、342 μmol/L非结合胆红素、0.03 g/L维生素C、5 g/L血红蛋白浓度、1 450 FTU乳糜对高、低值血清样本检测结果均无干扰。
测定240名健康人(男120名、女120名)空腹血清尿素浓度,测定数据经分析呈正态分布,总检测参考区间为1.4~7.2 mmol/L。
尿酶偶联谷氨酸脱氢酶速率法检测尿素的原理是在尿素酶催化下,尿素水解生成氨和二氧化碳,氨在α-酮戊二酸和还原型β-烟酰胺腺嘌呤二核苷酸存在下,经谷氨酸脱氢酶催化生成谷氨酸,同时还原型β-烟酰胺腺嘌呤二核苷酸被氧化成氧化型。还原型β-烟酰胺腺嘌呤二核苷酸在340 nm波长处有吸收峰,其 A值下降的速度与待测样本中尿素的含量呈正比[ 8]。此法特异性高、快速、结果准确精密,是目前测定尿素的首选方法。但我们在实际工作中发现,同样是酶法,R1和R2中的各成分分布不同对试剂的检测限和分析敏感性有较大影响。本研究对现有酶法尿素检测试剂进行了改良并对其性能指标进行了评估。结果表明改良试剂检测限为0.014 mmol/L,分析敏感性为-0.13,优于现有试剂及和光试剂,其空白 A值为1.8,空白 A值变化率为-0.001 9,与现有试剂相当。改良试剂对高、低值血清的批内精密度分别为0.45%和0.85%,批间精密度分别为0.38%和0.71%;线性范围为0~38 mmol/L;与和光试剂的比对, r=0.999,二者结果具有良好的可比性;342 μmol/L结合胆红素、342 μmol/L非结合胆红素、0.03 g/L维生素C、5 g/L血红蛋白、1 450 FTU乳糜对高、低值血清样本检测结果均无干扰。因此,改良酶法尿素试剂具有更加优越的检测限和分析敏感性,并且自身性能良好,与公认的优质进口试剂之间具有良好的相关性,符合临床应用要求。但从试验结果可见,无论是现有试剂还是改良试剂,其空白 A值变化率均不如和光试剂,推测这与我们所使用的原料有轻微氨污染有关,下一步可以从原料方面把关,以进一步提高试剂的相关性能。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|