通讯作者:王治国,联系电话:010-58115054。
作者简介:肖亚玲,女,1990年生,硕士,主要从事临床检验诊断学实验室质量管理研究。
评估全国甲状腺激素项目的检测性能。
方法用室间质量评价(EQA)数据估计各实验室结果与靶值的差值百分数,室内质量控制(IQC)数据[变异系数( CV)]评估不精密度。使用我国EQA评价标准和基于生物学变异的标准计算各项目差值百分数和不精密度的合格率,根据公式西格玛(σ)=[允许总误差(TEa)-偏倚(bias)]/ CV计算各检测项目的σ水平,绘制散点图,分析σ水平的分布。
结果促甲状腺素(TSH)项目 CV均值和差值百分数中位数最低,而三碘甲腺原氨酸(T3)项目最高。无论使用何种标准计算 CV和差值百分数的合格率,TSH项目的合格率都比其它项目高,而甲状腺素(T4)项目合格率最低。T4项目σ水平散点图的散点位置整体比其它项目低,分别有63.0%和98.2% σ<3;而TSH项目整体比其它项目高,分别有75.6%和72.9% σ≥3。
结论σ水平分析是一种简便直观的评价分析性能的方法,甲状腺功能检测项目中TSH项目检测性能优于其它项目,而T4项目检测性能低于其它项目。
To evaluate the performance of thyroid hormone testing all over the country.
MethodsThe difference percentage between results and target values was estimated according to external quality assessment (EQA) data, and the imprecision was obtained according to internal quality control (IQC) data [coefficient of variation ( CV)]. The EQA evaluation criterion in our country and biological variation quality specification were used to analyze the acceptabilities of difference percentage and imprecision in each group. The sigma (σ) value was calculated with the formula of σ=[total allowable error (TEa)- bias]/ CV. The scatter diagram was drawn, and the distribution of σ value was analyzed.
ResultsThe mean of CV and the median of difference percentage for thyroid stimulating hormone (TSH) were the lowest of all, while those for triiodothyronine (T3) were the highest. Regardless of quality specifications, the acceptabilities of imprecision and difference percentage for TSH were the highest, and those for thyroxine (T4) were the lowest. The scatter of T4 in the scatter diagram of σ value was entirely low, 63.0% and 98.2% σ<3. However, that of TSH was entirely high, 75.6% and 72.9% σ≥3.
Conclusionsσ value is a simple and visible method to evaluate the testing performance. The performance of TSH is better than the others, but T4 is worst of all.
甲状腺疾病是内分泌系统的常见疾病, 分为甲状腺功能异常和甲状腺本身疾病。甲状腺功能异常可以通过检测甲状腺激素来诊断。西格玛(σ )在数理统计中表示“ 标准差” , σ 水平则代表过程每百万次操作的缺陷概率, 其水平越高, 过程满足顾客要求的能力就越强。6σ 质量水平代表每百万次操作只允许3.4次超出规格界限, 或者说缺陷率为3.4× 10-6。6σ 管理法在临床检验中的应用最早由Nevalainen等学者提出, 可利用公式σ =[允许总误差(total allowable error, TEa)-偏倚(bias)]/变异系数(coefficient of variation, CV)计算σ 值和不精密度[1]。本研究中用实验室结果与靶值的差值百分数来代替bias进行σ 计算[2]。σ 值越大, 表示检测性能越好。我们将使用σ 水平对甲状腺功能项目的检测性能进行分析。
参加卫生部临床检验中心 2013年第1次内分泌项目室间质量评价(external quality assessment, EQA)计划, 且已回报2013年2月室内质量控制(internal quality control, IQC)数据的实验室。分析的项目包括:三碘甲腺原氨酸(triiodothyronine, T3)、游离T3(free triiodothyronine, FT3)、甲状腺素(thyroxine, T4)、游离T4(free thyroxine, FT4)和促甲状腺素(thyroid stimulating hormone, TSH)。
1.数据采集 向参加实验室发放5个批号的冻干质控品, 实验室复溶时准确加入5 mL去离子水或蒸馏水, 加盖室温放置30 min后轻摇混匀方可使用。利用基于Web方式的EQA软件上报5个样本的结果, 同时通过该软件网络上报其2013年2月的IQC数据。选择具有EQA和IQC数据的实验室进行分析, 内容包括:实验室编号、实验室名称、方法、仪器、试剂、校准品、IQC的CV、EQA结果。
2.不精密度评估 将各实验室上报的CV作为该室的不精密度水平评估。将各实验室CV与EQA评价标准以及基于生物学变异的允许不精密度[3]进行比较, 计算在不同要求下各项目CV的合格率。见表1。
3.差值百分数评估 将各实验室按照其上报的方法进行分组, 计算相同方法组每个批号上报结果的平均值, 作为该组该批号的靶值, 计算每个实验室结果与本组靶值之间的差值百分数, 将5个差值百分数的绝对值的平均值作为该实验室的差值百分数评估, 然后使用基于生物学变异的允许bias, 计算不同要求下各项目差值百分数的合格率。见表1。
| 表1 EQA评价标准和基于生物学变异的评价标准(%) |
4.σ 水平分析 分别使用EQA标准的TEa以及基于生物学变异的适当的TEa作为质量目标, 利用公式σ =(TEa- bias)/CV, 将方法的不精密度、差值百分数和TEa代入, 得到各实验室各项目的σ 水平, 并通过分布表和散点图分析σ 水平的分布。
采用SPSS 19.0软件和Excel软件进行统计分析。使用3次剔除超过3倍标准差(s)的方法剔除离群值。分别对每个项目的CV和差值百分数采用Kolmogorov-Smirnov (K-S)正态性检验。若P< 0.05则说明数据呈非正态分布, 采用中位数(四分位数间距)表示; 若P> 0.05则说明数据呈正态分布, 采用
对每个项目所有实验室的CV进行K-S正态性检验, 检验P值均> 0.05, 说明数据呈正态分布, 所以用x± s表示, 见表2。5个项目中CV均值最小的为TSH项目, 最大的为T3项目。所有项目CV的s均较大, 说明参加各实验室之间的CV水平差别较大。根据EQA评价标准和基于生物学变异的评价标准计算的CV合格率结果见表3。无论使用何种标准, 在5个项目中TSH的合格率要高于其它项目, 而T4项目合格率最低。如果使用1/3 TEa标准, 除了T4项目合格率为62.1%, 其它几个项目接近80%或高于80%。
| 表2 各项目CV统计结果及检验P值 |
| 表3 基于不同评价标准的CV的合格率(%) |
对每个项目所有实验室的差值百分数进行K-S正态性检验, 检验P值均< 0.05, 说明数据呈非正态分布, 所以用中位数(四分位数间距)表示。5个项目中差值百分数中位数最小的为TSH项目, 最大的为T3项目。根据基于生物学变异的评价标准计算的差值百分数合格率结果见表4。无论使用何种标准, T4项目的合格率均低于其它项目, 而TSH项目的合格率高于其它项目。
| 表4 各项目差值百分数统计结果和合格率 |
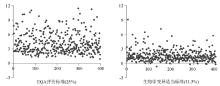
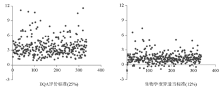
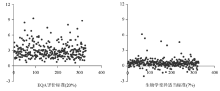
使用EQA评价标准的TEa和基于生物学变异的适当TEa分别计算各实验室的σ 水平, 其在各范围内的分布见表5。并绘制各项目σ 水平的散点图, 见图1~图5。从图中可以看出FT3、 T3和FT4项目EQA评价标准的σ 水平分布较分散, 3~6区间为散点较多的区域; 而生物学变异适当标准分布较集中, 将近90%集中在0~3区间内。T4项目EQA评价标准的σ 水平约有60%分布于0~3区间; 而生物学变异适当标准分布较集中, 约85%集中在0~3区间内。TSH项目2种评价标准的散点图分布相似, 约有50%的散点分布于3~6区域内。无论使用何种评价标准计算所得σ 水平, T4项目的散点位置整体偏低, 而TSH项目整体偏高, 说明T4项目检测性能较差, TSH项目检测性能较好。
| 表5 基于不同评价标准的σ 水平分布情况(%) |
临床检验分析检测过程的性能主要是用方法的不精密度和bias来评估。不精密度可以通过IQC长期累积的在控CV获得, bias可以通过EQA计划、正确度验证计划和方法比对获得。对于不精密度的评估标准, 目前我国已经出台了有关生化项目和血液学项目的卫生行业标准[4, 5], 但是对于甲状腺激素的检测项目, 还未形成统一、正式的相关标准。本研究采用EQA评价标准的1/3 TEa和1/4 TEa以及基于生物学变异的允许不精密度要求计算了各项目在不同标准下的CV合格率。除1/3 TEa外, 其它要求的合格率普遍偏低, 基于生物学变异的标准对于评价我国目前TSH的检测不精密度过于严格。所以建立符合我国基本情况的TSH检测项目的性能标准迫在眉睫。
σ 水平分析是一种简便、直观的评价分析性能的方法, 不需要分别评价不精密度和bias, 通过σ 值就能反映检测性能, σ 值越大, 表示检测分析性能越好。6σ 表示世界一流水平, 意味着检验结果有较好的质量, 其性能较佳, 不需要花精力改善性能; 3σ 通常为可接受水平, 其检测性能可接受, 同时具有一定的提升空间; < 3σ 表示结果有问题, 需要改善检测性能, 否则就有产生差错的风险。σ 水平除了可以评价分析性能, 还可以用来指导IQC的设计。通常σ 水平越高, 需要的质控方法就越简便, 可使用最简便的质控规则和最少的质控测定数量; σ 水平越低, 质控方法检出误差就越困难, 需要的质控方法就越复杂[6]。
根据本研究的结果, 可以初步反映我国甲状腺激素FT3、T3、FT4、T4和TSH 5个项目的检测性能现状。TSH项目CV均值和差值百分数中位数均比其它项目低, 且两者的合格率比其它项目高, 从σ 散点图也可看出该项目σ 水平整体比其它项目高, 说明TSH项目的检测性能优于其它4个项目。T3项目CV均值和差值百分数中位数均比其它项目高, 但是由于 T4项目的评价标准比其它项目要严格, 所以T4项目的差值百分数和CV的合格率在5个项目中最低, 且σ 散点图中T4项目的σ 水平整体比其它项目低, 说明该项目检测性能比其它4个项目差。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|