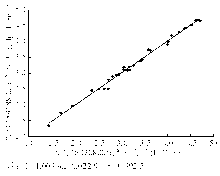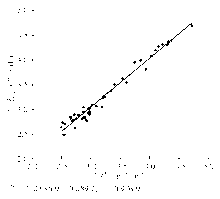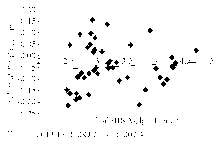评估罗氏和雅培公司乙型肝炎表面抗原(HBsAg)定量检测临床应用可行性。
方法收集423例血清和血浆标本,用雅培公司ARCHITECT HBsAg试剂和罗氏公司HBsAg quantitative Elecsys试剂进行比较检测,采用统计学方法分析两者之间的关系,并对2种试剂进行性能评估。
结果定量试剂的分析内和分析间变异系数(
2种HBsAg定量检测试剂在检测结果方面符合性较高,具有良好的相关性,其HBsAg检测结果可以互认。
To evaluate the clinical application feasibility of hepatitis B surface antigen (HBsAg) quantitative determination by Roche and Abbott.
MethodsA total of 423 serum and plasma samples were collected and determined by Abbott ARCHITECT HBsAg and Roche HBsAg quantitative Elecsys, and the results were analyzed comparatively. The correlation was analyzed statistically. Performance evaluation on Roche and Abbott was also conducted.
ResultsThe intra-analysis and inter-analysis coefficients of variation (
from Roche and Abbott HBsAg quantitative results are consistent and have a good correlation, and they are suitable for the clinical application. HBsAg results are consensus for each other.
两种方法检测HBsAg定量结果的临床互认研究
我国是乙型肝炎大国,长期以来,定量测定乙型肝炎病毒(hepatitis B virus, HBV)DNA为研究病毒水平与病情严重程度的关系、监测疾病进展和评价抗病毒药物疗效等提供了可靠依据[ 1, 2, 3]。但聚合酶链反应(polymerase chain reaction, PCR)操作技术较复杂,费用相对较高,对试验条件和操作人员的要求也较严格。近年研究表明,乙型肝炎表面抗原(hepatitis B surface antigen, HBsAg)定量结果和HBV DNA水平之间有良好的相关性,定量检测血清中HBsAg浓度可反映宿主体内HBV DNA的水平,动态监测HBsAg浓度变化对评价抗病毒治疗效果和预后具有重要意义[ 4, 5, 6, 7]。我们采用目前市场上主要的2种HBsAg定量试剂(罗氏和雅培)对423例血清和血浆标本进行比较研究,结合性能评估探讨其临床应用的可行性。
HBsAg标本均来自上海交通大学医学院附属第三人民医院感染科住院和门诊患者,共423例,其中临床确诊为乙型肝炎的阳性标本355例,浓度值分布在0.05~50 000 IU/mL;潜在干扰标本50例,为脂血、溶血、黄疸、类风湿因子阳性、孕妇血清等。另外收集HBsAg>250 IU/mL同一患者血清和血浆标本50份。
Abbott ARCHITECT i2000发光免疫分析仪及ARCHITECT HBsAg试剂(美国雅培有限公司);Roche Cobas e601发光免疫分析仪及HBsAg quantitative Elecsys试剂(德国罗氏诊断有限公司)。
分别采用罗氏公司和雅培公司的HBsAg定量试剂对HBsAg中、低浓度患者标本分别检测10次,计算变异系数(coefficient of variation, CV)值。
选择33例HBsAg阳性患者标本,分别用2个批号罗氏公司HBsAg定量试剂进行检测。收集HBsAg>250 IU/mL同一患者血清和血浆标本,共50份。用罗氏试剂对该血清、血浆标本进行同步检测。
将321份患者标本分别在Abbott ARCHITECT i2000发光免疫分析仪和Roche Cobas e601发光免疫分析仪上同步定量检测HBsAg含量。如果罗氏试剂初始检测结果超出检测范围,先对标本进行1∶100或1∶400自动稀释,再进行检测。如果雅培试剂初始检测结果超出检测范围,先对标本进行1∶25或1∶500手工稀释,再进行检测。
选取不含拟测试干扰物质的HBsAg阳性标本(用雅培试剂, 标本HBsAg浓度在120 IU/mL左右;用罗氏试剂,HBsAg浓度在65 IU/mL左右)50份和阴性标本50份。同一份标本分为2管,一管加入100 μL可疑干扰物(黄疸、溶血、脂血、类风湿因子阳性、孕妇血清各10例),另一管加入100 μL标本稀释液作为对照。干扰物质或稀释液加入前后,采用2种试剂连续检测10次。计算2次检测的偏差。
根据美国临床实验室标准化协会(Clinical and Laboratory Standards, CLSI) EP17-A文件的要求测定检测限。将罗氏HBsAg质控品进行系列稀释,直到低于检测下限,对稀释液和不含HBsAg的空白液进行系列检测,得出60个检测结果,这些值的第95百分位值为空白限。检测限由空白限和低浓度标本的标准差确定。
HBsAg的大部分标本都需要稀释后检测。雅培的HBsAg试剂检测范围0.05~250 IU/mL,超过上限可以手工稀释获得结果。罗氏的HBsAg试剂检测范围0.05~130 IU/mL,超过上限可以进行400倍自动稀释。选取一例高浓度HBsAg标本(>250 IU/mL),分别用罗氏和雅培试剂进行不稀释检测和稀释检测。对321例方法学对比检测结果进行检测结果区间分析,获取一般阳性标本的可报告范围。
以低值HBsAg质控液(0.15 IU/mL)为基础液,体积为1 000 μL,加入20 μL浓度为10 IU/mL的标本作为标准物质,用罗氏试剂和雅培试剂分别检测加入标准物质前后溶液的HBsAg结果。采用下列公式计算回收率。回收率=(A-B)/C×100%;A为加入标准物质的标本测得量,B为标本中该物质的测得量,C为加入的标准物质量。
采用SPSS17.0统计学软件对测定结果进行统计学分析,计算相关系数和回归方程, P<0.05为差异有统计学意义。
使用2个批号罗氏HBsAg定量试剂(分别为16070800和15918800)检测33例阳性标本。将33个检测结果先取自然对数,再进行相关性分析。统计分析显示2批次试剂检测结果有显著相关性(线性回归方程为 Y=1 .009 4 X-0.022 9, r=0.996, P<0.005),2批次试剂检测结果分布见图1:
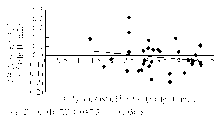
同时,对2个批次试剂检测结果作差值分析,发现差值均匀分布于坐标轴两侧,趋势方程为 Y=-0 .016 7 X+0.047 5,离散程度较小,经统计分析, P>0.05,2批次试剂检测结果的偏差分布见图2:
采用罗氏HBsAg定量试剂检测同一患者血清和血浆标本的HBsAg浓度,共50例患者。其中,3份标本检测结果超出检测上限,47份标本在线性范围内。对血清和血浆标本同时检测发现,结果的相关性良好(线性回归方程 Y=0 .986 9 X+0.089 2, r=0.988, P<0.05),具体结果分布见图3:
对血清和血浆检测结果做差值分析后发现,差值均匀分布于坐标轴两侧,趋势方程 Y=0 .013 1 X-0.089 2,离散程度较小,经统计分析, P>0.05,差值分布见图4:
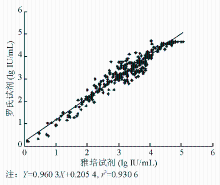
用雅培和罗氏试剂对321份标本进行比较试验,结果分布范围为1~50 000 IU/mL。将检测结果先取自然对数,再进行相关性分析,计算相关系数和回归方程。统计分析显示2种HBsAg试剂检测结果之间有明显相关性(线性回归方程 Y=0 .960 3 X+0 .205 4, r=0.965, P<0.05),具体检测结果的分布见图5:
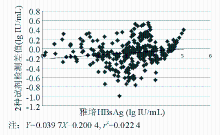
同时,对2种试剂检测结果进行差值分析,发现差值均匀分布于坐标轴两侧,趋势方程 Y=0 .039 7 X-0.022 4,离散程度较小,经统计分析, P>0.05,2种试剂检测结果差值分布见图6:
50份HBsAg阳性标本和50份阴性标本加入可疑干扰物(黄疸、溶血、脂血、类风湿因子阳性、孕妇血清各10例)前后的检测结果分析表明,HBsAg阴性标本加入上述干扰物前后,采用雅培或罗氏试剂检测结果都为阴性(<0.05 IU/mL),检测的偏差为0。对50例HBsAg阳性标本加入干扰物前后检测的差值进行分析,干扰物加入前后,罗氏试剂和雅培试剂检测结果一致,干扰物加入前后与对照稀释液比较,检测差值结果相一致。添加干扰物与添加阴性稀释液效果相同。见表2~表6:
| 表2 加入黄疸标本的偏差分析(IU/mL) |
| 表3 加入脂血标本的偏差分析(IU/mL) |
| 表4 加入溶血标本的偏差分析(IU/mL) |
| 表5 加入类风湿因子阳性标本的偏差分析(IU/mL) |
| 表6 加入孕妇血清标本的偏差分析(IU/mL) |
采用罗氏和雅培HBsAg定量试剂对比检测HBsAg低浓度稀释液和空白液,2种试剂的检测限均为0.05 IU/mL。
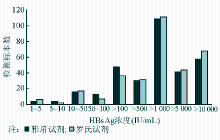
对高浓度HBsAg标本(>250 IU/mL)的不稀释检测,罗氏和雅培2种试剂的检测结果都显示超出上限(罗氏试剂:>130 IU/mL;雅培试剂:>250 IU/mL)。经过稀释后,罗氏和雅培试剂进行了20次重复检测,检测结果第95百分位数分别为945.8 IU/mL(罗氏试剂)和1 039 IU/mL(雅培试剂)。321例标本方法学对比检测结果区间分析表明,罗氏和雅培2种试剂检测区间内的标本数目非常接近,均处于稀释后报告结果范围内。区间分析还发现,10 IU/mL以下的标本所占标本比例为2.5%,1 000 IU/mL以上标本占全体标本的比例最大,达到了66%以上。提示400倍稀释检测对于大部分标本是有效措施。标本检测结果区间分析见图7:
罗氏和雅培的HBsAg试剂回收率计算结果分别为98%和102%,处于95%~105%区间内,2种试剂回收率性能评估保持一致。
1971年,Engvall等[ 8, 9]描述了检测HBsAg的酶免疫测定法。1976年,Wisdom研发了一种微粒“夹心”酶免疫测定法,HBsAg与包被抗HBsAg多克隆抗体微粒结合,然后与一种酶结合的乙型肝炎表面抗体(抗HBs)进行检测[ 10]。到1980年,研发出了以抗HBs单克隆抗体为基础的HBsAg检测方法[ 11, 12]。近来,对血清中HBsAg定量检测有了迅速发展,化学发光法因其操作简单、检测稳定、检测速度快、自动化程度高等优点,逐渐成为HBsAg常用检测方法[ 13]。
本研究采用2种进口化学发光试剂进行比较,判断2种试剂的临床应用性能。雅培和罗氏公司2种试剂虽同属化学发光法,但各自方法学仍有差异。雅培试剂在临床使用较广,是采用包被抗HBs单克隆抗体微粒子进行化学发光免疫测定。罗氏试剂刚在临床使用,是采用包被抗HBsAg单克隆抗体进行电化学发光免疫测定。其HBsAg定量标准都溯源到英国国家生物制品检定所参考标准、世界卫生组织国际标准(ad亚型),类似方法学、相同溯源标准是检测结果应具有相关性的基础。
从精密度水平来看,雅培HBsAg定量试剂 CV值约为5%,罗氏HBsAg定量试剂 CV值约为3%。对罗氏试剂的精密度检测发现, CV值为1.17%~1.30%,且不同批次试剂之间的批间差很小,不存在统计学差异,所以我们认为2种试剂的精度能满足临床使用的需要。
雅培和罗氏试剂对潜在干扰标本的检测结果显示,对于脂血、溶血、黄疸、孕妇血清、类风湿因子阳性的标本,2种试剂抗干扰能力相同。同时,我们研究了不同类型标本检测结果的差异。研究表明源自同一患者的血清和血浆标本的检测结果具有良好的相关性,说明不同标本采集方法对结果没有影响。
用罗氏和雅培试剂对患者标本进行检测,发现定量检测结果分布在1~50 000 IU/mL范围时,2种试剂检测结果之间具有良好的相关性,经过差值分析发现,2种试剂检测结果之间的差异也没有统计学意义,说明2种试剂的检测结果之间具有良好的互换性。
总之,雅培和罗氏2种HBsAg定量检测试剂具有良好的性能,能满足临床应用的需要。2种试剂的检测结果具有互认的特点。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|