作者简介:钱俊,女,1971年生,学士,主管技师,主要从事临床免疫学检验工作。
促甲状腺激素(thyroid stimulating hormone,TSH)是由腺垂体嗜碱细胞中的S-细胞分泌的一种糖蛋白激素,其值随正常的生理活动相应波动,是反映甲状腺功能的一个最敏感的指标[ 1]。妊娠期合并甲状腺功能亢进症(简称甲亢)的发生率约为0.02%~0.2%[ 2],合并甲状腺功能减退症(简称甲减)的发生率约为0.05%~2.3%[ 3, 4, 5, 6], 妊娠期并甲亢或甲减易造成流产、早产、胎儿生长受限、死产等,是引起孕妇和胎儿死亡率升高的一个重要原因,因此准确定量妊娠妇女血清中TSH的水平对于孕妇和胎儿的健康具有重要意义。目前,国内TSH的定量分析大多采用的是进口的电化学发光(electro-chemiluminescence, ECL)试剂。国内研发的光激化学发光(light initiated chemiluminescence assay,LiCA)检测TSH等项目的试剂于近年问世[ 7, 8, 9]。我们评价了国产LiCA TSH定量检测试剂的临床应用性能,并与ECL TSH检测试剂做比较,以探讨前者的临床适用性。
1. 样本 2011年10月26日至11月1日,上海市国际和平妇幼保健院产检孕妇的TSH血清样本384份。
2. 仪器 博阳LiCA HT和SP化学发光免疫分析仪;Roche E170 ECL免疫分析仪。
3. 试剂 Roche ECL TSH检测试剂盒(批号163973-01),参考区间为0.27~4.2 μIU/mL;博阳 LiCA TSH检测试剂盒(批号A1013),参考区间为0.4~4.51 μIU/mL。
1. 分析敏感性 方法参考EP17-A文件[ 10],质控在控的情况下,同批LiCA TSH试剂一次运行空白样本或零值校准品20次,计算均值( 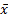
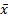
2. 功能敏感性 参考美国国家临床生化学院(NACB)检验医学应用准则[ 11] 中的功能敏感性测定方案,使用≥2批以上的试剂,在6~8周的时间内盲测不低于10例且涵盖整个分析范围的人血清样本,共20 d,每天测1次,每次复孔。以此方法计算变异系数( CV)为20%时对应的浓度值,即为该方法检测的功能敏感性。
3. 批内精密度 参考EP5-A2文件[ 12],采用同一批试剂、校准品,以各自配套的质控血清作为测试样本,一次运行对样本重复测定至少20次。计算 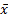
4. 线性 参考EP6-A文件[ 13]线性参数验证方案,采用高低浓度样本倍比稀释混合,在已知线性范围内选择5~7个浓度水平,每个浓度测3~4次。以样本号为 X轴,测定均值为 Y轴,做图进行回归分析。样本的制备按照等浓度间隔设计,见 表1。
| 表1 5个浓度水平的样本制备 |
5. 混合回收 待测样本等体积分为3份,取2份分别以等体积与高、低浓度质控品(QCH和QCL)等体积混合,分别测定待测样本、混合后样本、QCH和QCL各测3次,取 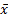
6.干扰 参考EP7-A文件[ 14]的配对差异法测定干扰影响。试验样本制备:分别向QCL和QCH中加入一定量干扰物储存液,使得其干扰物浓度为检测所允许的最大干扰物浓度,即血红蛋白为250 mg/dL,胆红素为10 mg/dL,甘油三酯为500 mg/dL;对照样本制备:分别向QCL和QCH加入与干扰物储存液相同体积的干扰物储存液的溶剂;交替测定试验样本和对照样本,每份样本重复测5次;由(试验样本 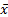
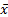
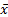
7.方法学对比 同一天内分别采用LiCA TSH检测试剂盒和ECL TSH检测试剂盒对384例样本进行检测。
试验数据采用SPSS 11.5软件进行统计学分析,采用配对 t检验对两系统的TSH定量结果做回归和相关性分析, χ2检验对定性结果做一致性分析, P<0.05表示差异有统计学意义。
LiCA的分析敏感性和功能敏感性分别为0.001 1和0.017 μIU/mL。
LiCA检测QCL和QCH的批内精密度分别为1.42%和1.55%,ECL检测QCL和QCH的批内精密度分别为1.50%和1.20%。
采用LiCA测定1~5号样本的TSH水平分别为0.02、27.33、51.52、77.60和97.82 μIU/mL,做回归分析, Y=24.58 X-22.9( r=0.998, P<0.05)。
测得待测样本、QCL和QCH浓度分别为0.51、0.83、20.52 μIU/mL,待测样本与QCL等体积混合后的样本为样本1,测得TSH浓度为0.65 μIU/mL,回收率为97.01%;待测样本与QCH等体积混合后的样本为样本2,测得TSH浓度为10.68 μIU/mL,回收率为101.57%。
干扰试验测定结果见 表2。所有干扰值均落在对照样本 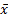
| 表2 LiCA干扰试验数据 |
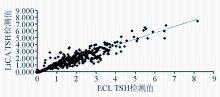
以ECL检测结果为基准,同时用LiCA检测384例血清样本的TSH值并做配对 t检验,结果差异无统计学意义( P>0.05);做回归分析, Y=0.923 X+0.205( r=0.906 5, P<0.05)。见 图1。
1. 敏感性、特异性以及总符合率 384例血清样本以ECL TSH检测结果为判定标准,LiCA TSH诊断甲亢的敏感性、特异性和总符合率分别为100.00%、98.61%和98.70%;诊断甲减的敏感性、特异性和总符合率分别为78.95%、100.00%和98.96%。
2. LiCA与ECL的一致性评价 将384例血清样本以ECL检测结果为参照做四格表,LiCA和ECL检测系统的甲亢判断限分别为<0.27和<0.40 μIU/mL;甲减判断限分别为>4.20和>4.51 μIU/mL,结果见 表3、 表4。经统计分析显示,2种方法在TSH的一致性判断上差异无统计学意义( 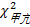
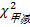
| 表3 LiCA和ECL甲亢诊断结果比较(例) |
| 表4 LiCA和ECL甲减诊断结果比较(例) |
ECL是将在电极表面引发的特异性化学发光反应同免疫测定相结合的分析方法[ 15],以Roche为代表。LiCA是继发光氧通道免疫分析(luminescent oxygen channeling immunoassay, LOCI)技术问世之后,在国内建立、发展并应用于临床检测的一种新型检测技术[ 16]。其检测原理简而言之就是“结合则发光”,该技术以其独特的检测方法,实现了均相、一步、免洗和高通量检测,在保持高敏感性、高特异性的同时彻底避免了清洗和分离所带来的误差,是标记免疫技术发展进程中一个新的里程碑。
正常人的甲状腺功能会随着年龄、性別和环境的改变而发生一定的变化。TSH在血清中的含量很低,临床上一般对于甲状腺功能紊乱患者的治疗需要监测6~8周的TSH水平变化,所以要求TSH检测方法有着相对比较高的批间精密度和敏感性,能够在TSH低值水平区分非甲状腺疾病和甲亢[ 17, 18]。本研究对LiCA TSH定量试剂盒的分析性能进行评估,发现其具有优异的分析敏感性、精密度、线性、混合回收和抗干扰能力,尤其是功能敏感性,LiCA为0.017 μIU/mL,与Roche TSH说明书标示的功能敏感性(0.014 μIU/mL)非常接近,这表明国产LiCA TSH定量检测试剂临床分析性能优异。
另外,本研究还对384例孕妇TSH的结果作对比,定量相关性优异,临床符合率无差异:384例样本中有5例样本在甲亢的判定上有差异,4例样本在甲减的判断上有差异,经分析发现都是由于试剂的参考区间设定的不同而造成的判定差异。
综上所述,国产LiCA试剂性能与进口ECL试剂无差异,且LiCA试剂有均相、免清洗和试剂成本较低等优点,适合用于临床。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|