作者简介:徐维家,男,1953年生,主任技师,主要从事自身免疫及分子生物学研究。
系统性红斑狼疮(systemic lupus erythematosus, SLE)是一种典型的系统性自身免疫性疾病,其特征是体内产生多种自身抗体,临床表现多样,难治愈,易反复。SLE易感基因是SLE发病的基础,自身免疫耐受的破坏,多克隆自身免疫反应性淋巴细胞增生及自身抗体的产生是SLE发病的中心环节。因而T细胞介导的自身免疫反应在SLE发病过程中发挥了重要作用。众所周知,辅助性T细胞1(Th1)及辅助性T细胞17(Th17)功能失调引起严重炎症反应并诱导产生多种自身免疫性疾病,且已有研究证实这2种细胞及其细胞的细胞因子在SLE的病情发展中起重要作用[ 1, 2]。我们通过检测SLE患者外周血Th17、Th1细胞及相关因子表达水平,探讨Th17与Th1细胞平衡动态变化及其在SLE发病中的意义。
选择大连市中心医院2011年5月至2012年3月门诊和住院的SLE患者38例,其中男4例、女34例,年龄(40±13)岁,SLE的诊断符合美国风湿病学会1997年制定的SLE分类诊断标准[ 3],病程为0.5个月~14年,平均病程(5.03±4.89)年。根据SLE活动指数(SLEDAI)评分[ 4]将患者分为活动组(≥10分)20例和非活动组(<10分)18例。 选择同期大连市中心医院健康体检者20名作为对照组,男3例,女17例,年龄(40±11)岁。2组对象一般资料比较差异无统计学意义( P>0.05)。
固定破膜剂IntraPrepTM、异硫氰酸荧光素(FITC)标记抗人CD3单克隆抗体、 藻红蛋白青色素5.1(PC5)标记抗人CD4单克隆抗体购自美国Beckman公司;藻红蛋白(PE)标记抗人白细胞介素17(IL-17)单克隆抗体、 PE标记抗人干扰素(IFN-γ)单克隆抗体购自美国eBioscience公司;佛波酯(PMA)、离子霉素(Ionomycin)、莫能霉素(monensin)购自美国Sigma公司;IL-17、白细胞介素23(IL-23)和IFN-γ的酶联免疫吸附试验(ELISA)试剂盒购自美国R&D公司。EPICS XL流式细胞仪(美国Beckman-Coulter公司),瑞典SUNRISE酶标仪。
受检者均于入院后第2天清晨空腹采集静脉血6 mL于肝素抗凝管中。密度梯度离心法分离外周血单个核细胞(PBMC)用于Th17和 Th1细胞的流式检测;分离血清于-20 ℃冻存用于细胞因子检测。所有标本均无乳糜和溶血。
1. 流式细胞术检测Th17和Th1细胞 将CD3-FITC和CD4-PC5单克隆抗体加入到分离出的PBMC中,混匀,避光室温孵育20 min,用RPMI-1640培养液洗涤后,将细胞加入到RPMI-1640培养体系中(含10%新生牛血清、50 ng/mL PMA、1 μg/mL离子霉素、3 μmol/L 莫能霉素),稀释细胞终浓度至1×106/mL,37 ℃培养箱中孵育18 h。将培养后的细胞用磷酸盐缓冲液(PBS)洗2次,用固定破膜剂进行固定、破膜(按试剂盒说明书操作)后加入PE-抗人IL-17和PE-抗人IFN-γ,对照管加入同型对照抗体,孵育30 min,洗涤后,应用流式细胞仪检测Th17 (CD3+、CD4+、 IL-17+)和Th1(CD3+、CD4+、IFN-γ+)细胞。
2.ELISA检测血清IL-17、IL-23和 IFN-γ水平 严格按照ELISA试剂盒说明书操作。
用SPSS 12.0统计软件进行分析,数据以 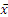
SLE组外周血中Th17细胞占CD4+T细胞的比例显著高于对照组( P<0.05),且SLE活动组Th17细胞的比例高于非活动组( P<0.05);而SLE组Th1细胞占CD4+T细胞的比例与对照组比较差异无统计学意义( P>0.05)。见 表1。
表1 各组外周血中Th17及Th1细胞的表达 (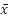 ±s) ±s) |
SLE患者外周血中Th17细胞比例与SLEDAI评分呈正相关( r=0.537, P<0.05),而Th1细胞比例与SLEDAI评分无相关性。
SLE患者血清IL-17、IL-23和IFN-γ水平较对照组升高 ( P<0.05);SLE活动组患者血清IL-17和IL-23水平较非活动组升高 ( P<0.05),而SLE活动组与非活动组患者的IFN-γ水平差异无统计学意义( P>0.05)。见 表2。
表2 SLE组和对照组血清IL-17、IL-23和IFN-γ水平比较(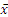 ±s,pg/mL) ±s,pg/mL) |
SLE患者血清IL-17、IL-23水平与SLEDAI评分均呈正相关( r=0.428、0.525 , P均<0.05),IFN-γ水平与SLEDAI评分无相关性。
SLE是一种复杂的因自身免疫调节功能紊乱而导致的多器官损害的自身免疫性疾病,越来越多研究表明CD4+T细胞在抵抗外来抗原中发挥重要作用,也与自身免疫性疾病密切相关。天然CD4+T细胞在不同细胞因子环境中激活可分化为不同的T细胞亚群,Th1细胞主要产生IFN-γ、白细胞介素2(IL-2)和肿瘤坏死因子β(TNF-β),过去一直认为自身免疫性疾病的发生与Th1细胞及细胞因子有重大关系[ 5]。然而自从发现了Th17细胞以后,人们已充分认识到Th17及其细胞因子IL-17与自身免疫的关联尤为密切,Th17细胞及其细胞因子参与多种自身免疫性疾病的发生过程,与许多自身免疫性疾病的发病都有重大关系[ 6]。
本研究显示,SLE患者外周血中Th1细胞比例与对照组无差异,而Th17细胞的表达高于对照组,且活动期Th17细胞数量高于非活动期,Th17细胞表达的升高导致Th17/Th1的比值也随之升高,与国内外大多数研究相一致。有学者指出Th17细胞在转化生长因子β(TGF-β)的诱导下产生IL-17,两者共同活化κβ核因子(κβNF),因此便起始了丝裂素活化蛋白激酶(MAPK)级联反应并刺激产生孤核受体(ROR)转录因子,由此导致了很强的致炎效应;同时募集巨噬细胞和中性粒细胞,加强炎症反应[ 7]。在研究Th17细胞的同时也要考虑Th1细胞的功能,因为Th1的细胞因子IFN-γ对IL-17的产生有抑制作用。本研究SLE患者的Th17表达升高,而Th1的表达与对照组无差异,打破了Th17/Th1之间的平衡,说明SLE患者的Th17应答增强。最近有学者通过实验得出结论,Th17细胞的应答受局部细胞因子环境的影响,在一定条件下不仅只产生IL-17,而且能产生Ⅰ类细胞因子如IL-2、肿瘤坏死因子α(TNF-α)和IFN-γ等,在病情的非活跃期Th17细胞可能向Th1细胞转化;然而在SLE活跃期Th17细胞却能抑制Th1细胞的作用[ 8],进而导致SLE活跃期时Th17/Th1平衡向着Th17方向偏移,本研究也得到相似的结论。
同时本研究显示血清中Th17的细胞因子IL-17水平显著升高,且在疾病活动期的表达也高于非活动期,并与SLEDAI评分亦呈正相关,显示两者与SLE发病机制有一定关系。Mok等[ 9]研究显示Th17浸润在SLE患者的各种器官中并分泌IL-17,进而诱导下游炎症因子维持炎症反应,这与本研究结果一致。曾有学者证明IL-17 通过诱导PBMC中IgG和抗dsDNA 抗体的过度表达来介导狼疮肾炎的发病机制[ 10]。IL-l7还可促进成纤维细胞和上皮细胞分泌趋化因子和其他细胞因子,促进炎性细胞向肾组织的招募[ 11]。本研究中IL-17的高表达充分说明IL-17在SLE发病机制中发挥重要作用。然而,有许多证据不支持IL-17在SLE中的作用,有学者研究证实SLE患者外周血淋巴细胞中的IL-17 mRNA表达水平及血清中IL-17含量较对照组无升高,在SLE的发病机制中不发挥效应[ 12] 。由于SLE的发病机制非常复杂,IL-17在SLE中的确切作用还未定论,可能与肾脏等脏器损害有关,不同的患者群和模型中发病机制可能不同[ 13]。
此外,本研究中IL-23在SLE患者血清中的水平高于对照组,与SLEDAI评分呈正相关,显示了IL-23作为Th17最有力的调节因子,在促进和维持Th17细胞分化方面发挥了重要作用[ 9]。Kyttaris等[ 14]证实敲除 IL-23基因的狼疮小鼠不出现自身免疫反应和狼疮性肾炎等一系列免疫功能紊乱的表现,因此证实IL-23受体介导的信号转导在狼疮发病中具有重要作用。作者认为IL-23可能间接参与了SLE的发病机制,IL-23能够促进Th17细胞的增殖分化并维持其存活,进而Th17细胞分泌IL-17、IL-23等促炎因子来介导SLE的免疫过程,但其确切的致病机制还需深入研究来进一步确定。
Bettelli等[ 15]在实验性自身免疫性脑脊髓炎(EAE)的中枢神经系统(CNS)中细胞因子的动态表达证实, 在EAE的高峰期,CNS中有Th17及Th1细胞因子,IL-17峰出现在IFN-γ之前,而IFN-γ可在靶组织内持续较长时间,甚至在IL-17表达消失后仍有表达。本研究结果显示SLE患者血清IFN-γ水平确实高于对照组,但与SLEDAI评分并无相关性,可能与IFN-γ的持续效应有关。可见虽然IFN-γ与病情活动没有关联,但其也可能通过一定的方式参与自身免疫过程,具体的机制还需要进一步研究。
综上所述,Th17与Th1的免疫调节作用可能在SLE的发病机制中发挥关键的作用;同时其相关的细胞因子也参与了疾病的免疫过程。但Th17细胞在SLE免疫紊乱中的具体作用、Th1细胞可能的协同作用机制及这2种细胞之间存在着怎样的具体联系尚不清楚,因此还需要大量的研究进一步阐明他们的相互作用、免疫调节功能,从而为治疗自身免疫性疾病开辟新的道路。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|

