作者简介:荣扬, 男,1962年生,学士, 主任技师,主要从事临床感染免疫、肿瘤免疫、自身免疫及免疫方法学研究。
探讨光激化学发光法(LiCA)和酶促化学发光法测定甲胎蛋白(AFP)和癌胚抗原(CEA)结果的可比性,评估LiCA AFP和CEA检测试剂的分析性能。
方法依据美国临床实验室标准化委员会(NCCLS)和《体外诊断试剂临床研究指导原则》,评估LiCA AFP和CEA检测试剂的分析灵敏度、不精密度和线性;分别用2种系统定量检测血清AFP(406例)和CEA(442例),对结果进行统计学分析。
结果LiCA AFP和CEA检测试剂分析灵敏度分别为0.112和0.05 ng/mL;批内变异系数(
LiCA检测AFP和CEA具有较好的分析性能,与酶促化学发光法高度相关,能满足临床检测要求。
To investigate the comparability of the results of alpha fetoprotein (AFP) and carcinoembryonic antigen (CEA) measured by light initiated chemiluminescence (LiCA) and enzyme-enhanced chemiluminescence, and evaluate the clinical performances of LiCA AFP and CEA kits.
MethodsAccording to the documents of National Committee for Clinical Laboratory Standards (NCCLS) and
The analytical sensitivities of AFP and CEA by LiCA were 0.112 and 0.05 ng/mL. The within-run and between-run coefficients of variation (
The clinical performances of LiCA AFP and CEA are satisfied to clinical measurement. There is a correlation between the 2 systems for AFP and CEA.
纵观标记免疫分析的发展史,近年来,化学发光免疫分析已占据了免疫分析的主导地位,尤其是进口的化学发光试剂占据了相当的份额。光激化学发光免疫分析技术(light initiated chemilum-inescence assay,LiCA)[ 1]作为一种新型的国产化学发光免疫分析技术,与进口的酶促化学发光免疫分析技术在定量检测结果上是否具有可比性,是目前需要探究的问题。
甲胎蛋白(AFP)和癌胚抗原(CEA)[ 2]是临床常用肿瘤标志物。AFP由Abelev等于1963年发现,是一种胚胎蛋白[ 3, 4],在肝癌、胚胎细胞肿瘤、卵巢癌或睾丸癌患者血清中会明显升高。CEA于1965年由Gold和Freedmen从结肠癌患者血清中发现,在肿瘤生长和转移[ 5]中起重要作用;在非小细胞肺癌[ 6]、结肠癌、直肠癌及内胚层来源的其他肿瘤癌变时会明显升高。
我们评价了LiCA AFP、CEA定量检测的分析性能,并与酶促化学发光法检测试剂作了比较,以探讨前者的方法优势和临床适用性。
1.仪器与试剂
LiCA HT和SP化学发光免疫分析仪[博阳生物科技(上海)有限公司]及配套试剂(AFP、CEA试剂批号分别为A1010、A1016)。BECKMAN-COULTER DXi800化学发光免疫分析仪(酶促化学发光法,美国Beckman-Coulter公司)及配套试剂(AFP和CEA试剂批号分别为16688、195018)。
2.样本
取自中国人民解放军海军总医院临床血清样本,其中用于AFP测定406例,用于CEA测定442例。
1.分析灵敏度
评价方法参考美国临床实验室标准化委员会(NCCLS)EP17-A[ 6]文件。在质控在控的情况下,同批LiCA AFP/CEA试剂一次运行零值校准品20次,计算均值( 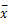
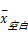
2.批内精密度
参考NCCLS EP5-A2[ 7]文件程序。采用同一批试剂、校准品以各自配套的2个水平质控血清作为测试标本,一次运行对标本重复测定20次,计算 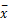
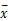
3.线性
参考NCCLS EP6-A[ 8]文件,选用已知高、低浓度2个样本等比例稀释成6个浓度水平,每个浓度测定6次,剔出离群点,计算 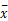
4.相关性分析
在质控在控的情况下,分别采用LiCA和酶促化学发光法同时检测AFP和CEA并做相关分析。
采用SPSS11.5软件对2种系统的AFP、CEA定量相关系数( r)进行统计学分析。
依据零值校准品测定值计算所得,LiCA AFP和CEA的分析灵敏度分别为0.112、0.05 ng/mL。
LiCA测定AFP和CEA的线性数据见 表2。对 表2数据做回归分析,得出方程: YAFP=0.99 XAFP+1.36, r=0.999; YCEA=0.98 XCEA+2.87, r=0.999。AFP线性范围为2.6~950.2 ng/mL,CEA线性范围为1.2~862.6 ng/mL。
| 表2 LiCA测定AFP和CEA的线性数据(ng/mL) |
以酶促化学发光法结果为基准,对406例AFP血清样本及442例CEA血清样本分别做定量相关分析,相关方程分别为 YAFP=1.027 XAFP-0.516, r=0.997; YCEA=0.821 XCEA+1.355, r=0.991,见 图1、2。
1959年美国学者Berson和Yalow用放射免疫法成功测定了血浆胰岛素[ 10],开创了标记免疫分析的新纪元。接着,各种新型的标记物的不断推出,使得标记免疫分析有了突飞猛进的发展:从放射免疫发展到无放射性污染的酶联免疫,再到灵敏度更高的荧光免疫,最后到易于自动化的发光免疫。化学发光免疫分析是上世纪90年代出现的标记免疫分析,根据其标记物的不同又分为直接化学发光、酶促化学发光、电化学发光和光激化学发光。
酶促化学发光[ 11]主要包括碱性磷酸酶(AP)系统、辣根过氧化物酶(HRP)系统等。美国Beckman-Coulter公司是AP系统的代表,其原理是采用磁性微粒为固相载体包被抗原或抗体,AP标记抗原或抗体,利用免疫反应使得AP同待测物结合到固相载体上,通过磁场分离、洗涤后加入底物金刚烷二氧环已烷(AMPPD),数分钟后测定发光强度来测定待测物的浓度。
光激化学发光作为一种新的化学发光免疫分析技术,是继单线态氧分子能量传递发光免疫分析技术[ 12](luminescent oxygen channeling immunoassay, LOCI)技术问世之后,在国内建立、发展并应用于临床检测的一种新型检测技术。其检测原理是以填充了感光和发光染料的2种200 nm的高分子纳米微球为载体分别共价交联抗原抗体,由免疫反应拉近感光和发光微球的距离至200 nm以内。当用680 nm激发光照射,感光染料被激活并释放高能态的单线态氧给发光染料,4 μs后发光微粒发出610 nm的光,根据光信号得到待检物的浓度,简而言之就是“结合则发光”。该方法属于均相免疫反应,相对于非均相免疫分析其实施难度更大,技术含量更高。
均相免疫反应是在抗原抗体反应过程中不需要清洗分离而在反应结束后直接测量信号的免疫分析方法。而在免疫分析中,清洗分离这一步骤所产生的误差占免疫分析总误差的70%~80%,如酶联免疫吸附试验(ELISA)等进行定量分析由于包被不均一性和清洗分离的不确定性,导致其不精密度和准确性不够理想。光激化学发光免疫分析技术因具有免清洗分离的特点,减少了清洗和分离所带来的误差,减少了反应时间,并且易于实现自动化和高通量检测[ 13]。因此,可以说LiCA技术是标记免疫技术发展进程中一个新的生力军。作为非均相免疫分析的代表之一,美国Beckman-Coulter公司的全自动化学发光因其先进的工艺使其分析过程的误差降到了很低的水平。而光激化学发光利用其免清洗技术实现了分析性能的可靠。
本研究对LiCA AFP和CEA定量检测试剂的临床性能做了评估,结果显示LiCA测定AFP和CEA在分析灵敏度、线性和精密度方面均可满足临床应用;与酶促化学发光法结果进行比对,2种检测系统高度相关( r>0.99)。由此可见LiCA检测AFP和CEA的分析性能可以满足符合相关标准要求;且具有均相免清洗、试剂成本较低等优点,因此能够应用于临床,满足广大临床实验室和患者的需求。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|