刘丽慧,女,1986年生,硕士,主要从事硫氧还蛋白还原酶肿瘤标志物临床检验研究。
曾慧慧,联系电话:010-82802878。
近年,全世界肿瘤发病率呈逐年递增趋势。2010 年全球有超过800 万人死于恶性肿瘤,癌症已取代心血管类疾病成为致死率最高的病症存在。随着肿瘤发病率的不断提高,肿瘤标志物检测在肿瘤诊治方面的重要作用被公认且受到临床的高度重视。硫氧还蛋白还原酶(thioredoxin reductase,TR)活性检测是针对体内异常增生的酶活性进行的检测。该酶本身敏感且是启动所有肿瘤相关蛋白工作的上游调控酶,相对肿瘤相关的其他蛋白类检测指标提前,从而达到肿瘤早期检测和针对肿瘤的发生起到控制的作用,可以作为新型肿瘤标志物用于恶性肿瘤的辅助诊断[ 1]。在日常临床检验工作中经常会遇到溶血标本,目前还没有不同溶血程度对TR活性检测影响的报道。我们通过人工制造溶血,并针对不同程度溶血对TR活性检测结果的影响进行对比分析。
选择武汉凯熙医学检验所正常体检者68例,空腹取静脉血标本,肝素钠抗凝,无溶血、脂血和黄疸。
Tris-HCl缓冲液(称取3.784 g三羟甲基氨基甲烷,用蒸馏水溶解移入500 mL容量瓶并稀释至刻度,以浓盐酸调节pH值至8.0,缓冲液的终浓度为62.5 mmol/L);TR活性检测试剂盒(武汉尚宜康健科技有限公司,批号20110901)。U-1800PC型紫外可见分光光度计(上海美普达仪器有限公司),Multiskan Mk3型酶标仪(Thermo Scientific公司),HC-2518R型高速冷冻离心机(安徽中科中佳科学仪器有限公司),DHP-9082型恒温培养箱(上海一恒科学仪器有限公司),Starter-3C 型pH计[奥豪斯仪器(上海)有限公司],AL104型万分之一电子天平[梅特勒-托利多仪器(上海)有限公司]。
每例血标本均取1.0~1.5 mL于800× g离心10 min,离心后分别取血浆200 μL,加入与之对应的100 μL血细胞并混合均匀。将血样进行反复冻融后,离心取上清,得68份溶血标本[ Ai(i=1,2……68)]。
以正常未溶血血浆作为正常对照组;将每例溶血标本和正常对照血浆以不同比例混合,按照测定后的血红蛋白(hemoglobin, Hb)浓度制备成Hb分别为1.0、2.0、3.0、4.0、5.0、6.0、7.0 、8.0 g/L的标本,共计68组8个梯度溶血标本。
将300 μL溶血标本A1加入到2.7 mL Tris-HCl缓冲液中配成溶液,用同浓度Tris-HCl缓冲液稀释40倍得溶液B1,然后用紫外可见分光光度计分别测定波长为450、415和380 nm处Hb的吸光度( A)值[ 2]。根据Allan公式[Hb(g/L)=1.68 A415 nm-0.84×( A450 nm + A380 nm)]计算Hb含量。
采用分光光度法进行酶活性测定,操作严格参照TR活性检测试剂盒说明书进行。根据试剂说明书标准判断结果:TR ≤ 4.0 U/mL表示无异常增生;TR>4.0 U/mL表示有不同程度异常增生。
溶液B1的 A415 nm =1.550、 A450 nm =0.267、 A380 nm =0.394,经过Allan公式计算,溶液B1中的Hb浓度为2.0 g/L。
不同程度溶血标本的TR检测结果见表1:
| 表1 不同程度溶血标本的TR检测结果(U/mL) |
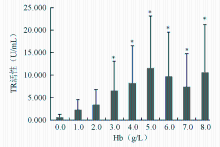
不同浓度Hb的溶血标本间TR均值比较见图1:
将Hb浓度为0.0~5.0 g/L的溶血标本的TR均值与不同浓度Hb做图,得到TR均值( Y)和Hb浓度( X)的线性方程: Y=2 .164 X+0 .034,线性回归系数( r)为0.988 0;表明Hb浓度在0.0~5.0 g/L范围内,TR均值与Hb浓度呈正比。见图2:
注: Y=2 .164 X+0 .034, r=0 .988 0
溶血是临床检测中最常见的一种干扰因素[ 3]。本研究结果表明,在Hb浓度分别为1.0、2.0 g/L的溶血条件下,TR活性仅轻微升高,没有超出TR正常范围,在Hb≥3.0 g/L的溶血条件下,TR活性明显升高(>4.0 U/mL),属于异常增生范围;当Hb浓度在0.0~5.0 g/L范围内,TR均值与溶血程度呈正比( r=0.988 0),在此范围内随溶血程度的增加,TR均值升高。在一定范围内溶血标本的 A值随溶血程度的增加呈逐渐升高的趋势,导致结果出现假阳性,其影响的机制大致可归纳为以下几方面:(1)红细胞破裂释放出Hb,Hb对300~500 nm波长光的吸收引起比色干扰,而TR活性检测在405 nm进行,Hb会对检测产生影响,引起 A值的改变;(2)红细胞内外液之间的各种反应导致检测结果改变;(3)红细胞破裂后一些高浓度的离子或酶等从细胞内释放出来,导致检测结果增高;(4)由于细胞破裂导致细胞内物质释放,而使血浆量增多,检测物被稀释。以上几个方面都有可能造成检测结果出现误差,产生假阳性。
综上所述,对于溶血标本不能一律作为不合格品拒收,特别是标本来源困难或者急需检测结果,可以接收对检测结果无明显差异的标本(Hb≤2.0 g/L)进行检测;如果溶血血浆标本Hb浓度达到2.0 g/L以上时,会对TR活性检测产生影响,此时测定出的TR活性的实际意义不大。建议重新采血检测,避免出现假阳性。
| [1] |
|
| [2] |
|
| [3] |
|