通讯作者:应春妹,联系电话:021-68383297。
作者简介:郑冰,女,1984年生,学士,技师,主要从事微生物检验工作。
分析仁济医院光滑念珠菌的基因分型以及不同基因型光滑念珠菌的药物敏感性结果,以了解仁济医院光滑念珠菌的耐药性和流行情况,并探讨两者间是否存在相关性。
方法运用多位点序列分型(MLST)技术,对34株光滑念珠菌的6个管家基因进行测序分析,利用Clustalx软件与MLST数据库进行序列比对,确定其等位基因谱型及菌株序列型(ST)。利用Clustalx软件绘制进化树,同时通过eBURST程序将菌株分为各个克隆系,以比较不同基因型之间亲缘关系的远近。采用ATB FUNGUS半自动真菌鉴定和药物敏感性分析系统进行药物敏感性试验,结合基因分型结果,运用Ridit分析方法探究两者的联系。
结果34株光滑念珠菌经MLST分型,得到6个ST,其中ST-7 27株,占总数的79.4%(27/34);ST-10 3株,占总数的8.8%(3/34),其余4型(ST-3、ST-15、ST-43、ST-55)各1株。34株光滑念珠菌对氟胞嘧啶、两性霉素B 100.0%敏感,对伏立康唑和氟康唑的敏感率分别为97.1%和91.2%,伊曲康唑抑菌效果差,敏感率仅11.8%。以ST-7为标准组,氟康唑、伏立康唑及伊曲康唑药物组中ST-10组及其他ST组均包含标准组的平均Ridit值。
结论ST-7为仁济医院光滑念珠菌中优势菌株;光滑念珠菌的耐药谱与基因型相关性差。
To investigate genotypes and drug susceptibility of
Multilocus sequence typing (MLST)technique was introduced to identify sequences of 6 housekeeping genes from 34 isolates of
The 34 isolates belonged to 6 clone sequences. ST-7 had the most proportion of 79.4%(27/34). There were 3 isolates belonged to ST-10, accounting for 8.8%(3/34), and the remaining 4 isolates belonged to ST-3, ST-15, ST-43 and ST-55, respectively. A total of 34 isolates of
ST-7 is the dominant genotype in Renji Hospital. No correlation between the
由侵袭性念珠菌引起感染的上升,已经成为一个严重的公共健康问题。随着免疫抑制剂在临床的广泛使用,免疫缺陷人群的增多,尤其是获得性免疫缺陷综合征疫情的蔓延,白念珠菌在临床的分离率有所下降,而非白念珠菌,尤其是光滑念珠菌等引起的感染明显增加[ 1]。抗真菌药物的大量应用使光滑念珠菌耐药株日益增多,耐药性已成为影响临床光滑念珠菌感染治疗效果的主要原因。对真菌快速准确地分型并分析该菌种间、种内的亲缘关系对研究真菌的致病性、药物敏感性和流行病学调查具有重要意义。
目前已经建立了多种光滑念珠菌的分子生物学分型技术,如扩增片段长度多态性分型(AFLP)、随机扩增多态性DNA分析(RAPD)、限制性片段长度多态性(RFLP)等。这些技术在研究病原菌的流行病学调查中都发挥了重要作用,但仍然存在一些不足,其中最主要的缺点是不同实验室间结果重复性较差。多位点序列分型(multilocus sequence typing,MLST)技术通过测序技术揭示管家基因等位基因突变来达到对病原菌进行分型和鉴定的目的,有利于不同实验室结果的相互比较,从而使分子流行病学结果更为标准化。本研究拟应用MLST系统对仁济医院不同科室分离的光滑念珠菌株进行基因水平分型,并与国际流行克隆株进行比较,同时结合光滑念珠菌的耐药性特征,对不同基因型的光滑念珠菌进行药物敏感性分析,以了解其相互之间的相关性。
1. 菌种来源 2010年仁济医院微生物室从33例深部真菌感染患者标本中分离得到34株光滑念珠菌(去除重复菌株),其中2株光滑念珠菌分别来自同一患者的血液和清创物标本。这些菌株临床科室分布为:神经外科10株,门诊4株,肝移植科3株,呼吸科3株,普外科3株,干部病房2株,外科监护室2株,消化科2株,神经内科、肾移植科、骨科、放疗科、心内科各1株。34株菌株分离自不同临床标本,其中痰21株,粪便4株,血液3株,引流液、咽拭、中段尿、颈静脉导管、棉拭、清创物各1株,见 表1。
| 表1 34株光滑念珠菌科室分布及标本来源 |
2. 主要试剂 菌种鉴定同时采用法国生物梅里埃公司的VITEK 32酵母菌鉴定卡(YBC)和API 20C AUX酵母菌鉴定板条;真菌DNA抽提试剂盒为Biospin Fungus Genomic DNA Extraction Kit (上海Bior, Cat;No: BSC14S1);聚合酶链反应(PCR)试剂购自TaKaRa公司;PCR反应引物由Invitrogen公司合成;目的基因片段送华大基因公司测序;药物敏感性试验采用由法国生物梅里埃公司生产的ATB FUNGUS半自动真菌鉴定和药物敏感性分析系统。
1. 培养鉴定 将保存的菌种转种于沙保罗培养基中,37 ℃培养2448 h,分纯后使用VITEK 32酵母菌鉴定卡(YBC)和API 20C AUX酵母菌鉴定板条同时鉴定,所有菌株经鉴定均为光滑念珠菌。
2. DNA提取 从沙保罗培养基中挑取35个菌落转入300 μL 生理盐水中,混匀,6 000× g离心3 min,收集沉淀。按照真菌DNA抽试剂盒Biospin Fungus Genomic DNA Extraction Kit操作步骤进行DNA提取,最后将抽提的DNA于-20 ℃保存备用。
3. PCR扩增 采用Dodgson等[ 2]推荐的方法确定光滑念珠菌基因组上的6个管家基因( FKS、 LEU2、 NMT1、 TRP1、 UGP1、 URA3)作为目的基因片段,见 表2。PCR反应采用25 μL体系,其中10×PCR缓冲液(含Mg2+)2.5 μL,2.5 μmol/L dNTPs 2 μL,10 μmol/L上游引物和下游引物各1 μL,5 U/μL TaKaRa Taq酶0.2 μL,模板DNA 1 μL,无菌蒸馏水加至25 μL。反应条件:94 ℃预变性7 min;94 ℃变性1 min,退火温度见 表2,退火时间1 min,74 ℃延伸1 min,共30个循环;74 ℃总延伸10 min。
| 表2 PCR扩增引物及退火温度 |
将PCR扩增产物用1.5%琼脂糖凝胶进行电泳,溴乙锭(EB)染色后于凝胶成像仪上判读结果,观察是否扩增出目的条带。扩增出的目的核酸片段由华大基因公司进行正反向测序。
4. MLST数据分析 通过Clustalx软件将6个管家基因测序结果与MLST数据库进行比对,获得各管家基因位点的等位基因数值,并形成相应的等位基因谱,判断其序列型(ST)。运用Clustalx软件绘制进化树,并通过TreeView软件查看。采用eBURST v3.0程序将菌株分为各个克隆系(clonal complex)。用于eBURST分析的相关ST数据来源于光滑念珠菌MLST网的公开数据库(http://cglabrata.mlst.net/eburst /database.asp)。
5. 药物敏感性试验 采用ATB FUNGUS半自动真菌鉴定和药物敏感性分析系统,按照操作说明进行试验,在37 ℃培养24 h读取药物敏感性结果,见 表3。
| 表3 5种抗真菌药物的判定标准(μg/mL) |
通过SPSS 13.0软件,运用Ridit分析法探究光滑念珠菌的基因型与药物敏感性之间的关系。
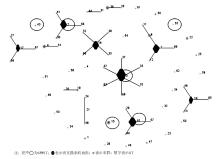
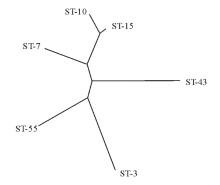
34株光滑念珠菌均扩增出6个管家基因( FKS、 LEU2、 NMT1、 TRP1、 UGP1、 URA3),各基因对应条带片段长度分别为589、512、607、419、616和602 bp。将每株菌的6个管家基因片段测序结果与MLST数据库进行比对,结果显示,34株光滑念珠菌得到了6个ST,其中ST-7 27株,ST-10 3株,ST-3、ST-15、ST-43、ST-55各1株。来自同一患者不同标本的2株光滑念珠菌均为ST-7。经eBURST v3.0分析发现,这6个ST分别来自不同的克隆系,见 图1。利用Clustalx软件对ST序列进行聚类分析,结果见 图2。
34株光滑念珠菌来源于仁济医院不同的临床科室,以神经外科分离率最高,占总数的29.4%(10/34);其次是门诊,占总数的11.8%(4/34);肝移植科、呼吸科、普外科各分离到3株,分别占总数的8.8%(3/34);干部病房、外科监护室、消化科各分离到2株,分别占总数的5.9%(2/34);神经内科、肾移植科、骨科、放疗科、心内科各分离1株,分别占总数的2.9%(1/34)。
结合光滑念珠菌基因分型结果发现神经外科分离的10株光滑念珠菌有7株为ST-7,占70%(7/10),其余3株分别为ST-55、ST-43、ST-10;门诊分离的4株菌株,3株为ST-7,占75%(3/4),1株为ST-3,占25%(1/4);呼吸科分离的3株菌株,2株为ST-7,占67%(2/3),1株为ST-10,占33%(1/3);外科监护室分离的2株菌株,1株为ST-7,1株为ST-10型,各占50%;肝移植科、普外科、干部病房、消化科、神经内科、肾移植科、骨科以及放疗科分离的菌株均为ST-7;心内科分离的1株菌株为ST-15。
34株光滑念珠菌对氟胞嘧啶、两性霉素B 100.0%敏感;对伏立康唑和氟康唑的敏感率分别为97.1%和91.2%;伊曲康唑的抑菌效果较差,敏感率仅为11.8%,见 表4。
| 表4 34株光滑念珠菌的药物敏感性试验结果 |
通过SPSS 13.0软件,运用Ridit分析方法分别比较ST-7、ST-10以及其他4型光滑念珠菌在氟康唑、伊曲康唑、伏立康唑的耐药性上是否存在差异。以ST-7为标准组,氟康唑药物组中ST-10组
伊曲康唑药物组,ST-10组
伏立康唑药物组,ST-10组
引起严重感染的条件致病真菌逐年增加,但在全球范围内最重要的致病菌仍是念珠菌属[ 3]。近年来,光滑念珠菌引起的感染明显增加。既往人们认为光滑念珠菌是人体黏膜组织的非致病性的共生菌,只是偶尔引起机会感染。继免疫疗法和广谱抗真菌预防在临床广泛使用,光滑念珠菌已经成为一个重要的条件致病菌。有报道显示,美国光滑念珠菌引起的血液感染约占念珠菌属菌血症的20%,欧洲约占15%,亚洲约占10%,拉丁美洲约占5%[ 4]。长期大剂量地应用抗真菌药物,使得光滑念珠菌耐药菌株日趋增多,由其引起感染的治疗相对困难,所致的系统性感染病死率较高[ 5]。因此,通过分子生物学分型方法对上海仁济医院光滑念珠菌进行流行病学研究并监测其耐药性,对控制传染源、防止耐药菌株增加以及预防院内大规模真菌感染的暴发流行具有重要意义。
MLST是近年来发展的、新的分子生物学分型方法,具有很高的分辨能力。真菌同一属或种中,管家基因几乎都存在保守性,同时以中等或较慢的速度进化,因此管家基因能很好地反映菌株间的系统发育关系。MLST通过分析多个管家基因内部片段的核苷酸序列对病原菌进行基因分型,通过MLST数据库能对不同实验室及不同国家的分析结果进行比较,还能够进行种群结构及生物进化方面的研究,适合于病原微生物的分子流行病学和分子进化学的研究。
本研究应用MLST方法对仁济医院临床分离的34株光滑念珠菌进行分型,6个管家基因( FKS、 LEU2、 NMT1、 TRP1、 UGP1、 URA3)作为目的基因研究。仁济医院临床分离的34株光滑念珠菌共获得了6个ST(ST-7、ST-10、ST-3、ST-15、ST-43和ST-55),分别属于不同的克隆系,并非单克隆播散。其中27株菌为ST-7,占总数的79.4%,因此ST-7为优势基因型。Lin等[ 6]将80株光滑念珠菌进行MLST,发现50株菌株分布于ST-7、ST-3、ST-10、ST-15和ST-26,24株为新的ST,其中以ST-7居多,占30%(24/80),这与我们的结果一致。我们还将MLST结果与标本类型进行比较,发现仁济医院分离自无菌部位的6株光滑念珠菌(3株来自血液,其余3株分别来自颈静脉导管、引流液和清创物)均为ST-7。Lott等[ 7]也将MLST技术用于光滑念珠菌研究,结果美国多个地区血培养中分离得到的230株光滑念珠菌以ST-16、ST-19和ST-3为主。因此,应用MLST能对光滑念珠菌进行有效分型和遗传分组,并可实现不同实验室试验分析结果之间的比较,为全球范围内大规模流行病学调查提供了基础。
其次,我们在这次研究中发现神经外科是仁济医院光滑念珠菌分离数量最多的科室,其ST分布以ST-7为主,其余ST-10、ST-43、ST-55各1株。且该病区有一位患者的血液和清创物标本在不同时期均分离到光滑念珠菌,经MLST均为ST-7,可认为是同一株菌株引起的不同部位的感染。神经外科成为仁济医院光滑念珠菌感染的重灾区可能与该病区患者长期使用广谱抗菌药物、糖皮质激素、频繁的侵袭性操作以及长期卧床有关。因此,该科室更应注重对具有侵袭性真菌感染高危因素患者的各项检查,根据药物敏感性试验结果使用窄谱抗菌药物,尽量避免不必要的侵袭性操作,以降低院内真菌感染的发生率。
对34株光滑念珠菌耐药性进行分析发现,其对伊曲康唑的耐药性较为严重,敏感性低,仅为11.8%,这与国内外文献报道较一致[ 11, 12]。光滑念珠菌对三唑类药物存在交叉耐药现象应引起关注。Wong-Beringera等[ 8]研究显示80%的耐氟康唑的光滑念珠菌同时对伊曲康唑耐药,24%的耐伊曲康唑的光滑念珠菌同时对氟康唑耐药。本研究未检测到对氟康唑耐药的光滑念珠菌,但3株对氟康唑中介的光滑念珠菌中有1株对伏立康唑和伊曲康唑均耐药,还有2株对伊曲康唑耐药,对伏立康唑敏感。由于光滑念珠菌对三唑类药物交叉耐药率高,临床分离的光滑念珠菌如对氟康唑耐药,则对伊曲康唑耐药的可能性较大,故在进行药物选择时应注意光滑念珠菌交叉耐药的特性。此外,目前由于临床上氟康唑大量使用,导致出现耐氟康唑的光滑念珠菌。Hazen等[ 9]研究发现光滑念珠菌对伏立康唑和氟康唑的耐药率明显上升,Pfaller 等[ 10]也得到相同的结果。由于光滑念珠菌对氟康唑的耐药率高,因此,氟康唑通常不作为治疗光滑念珠菌感染的首选药物。
我们还将MLST结果与药物敏感性试验结果相结合,运用Ridit分析方法分别比较ST-7、 ST-10以及其他4型光滑念珠菌对氟康唑、伊曲康唑和伏立康唑的药物敏感性上是否存在差异,结果发现不同基因型与药物敏感性之间差异无统计学意义。但是,要真正了解基因型与耐药性是否存在关联还需要进行不同分子生物学分型方法的更大规模的耐药分子流行病学调查,相信随着分子生物学技术的不断发展和临床各个科室对于深部真菌感染的不断重视,真菌的流行病学和耐药性监测将更有利于临床真菌感染治疗。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|