通讯作者:张秀明,联系电话:0760-88823566-22916。
作者简介:黄福达,男,1977年生,学士,副主任技师,主要从事临床血液及体液检验。
评价UF-1000i全自动尿液有形成分分析仪(简称UF-1000i)的性能。
方法参照美国临床实验室标准化协会(CLSI)H56-A文件及UF-1000i病例研究手册的性能评价方法对该仪器的5个定量分析参数的批内精密度、批间精密度、携带污染率、线性范围、不准确度、与镜检符合率等性能进行评价。
结果白细胞(WBC)、红细胞(RBC)、上皮细胞(EC)、管型(CAST)、细菌(BACT)的批内精密度分别为1.37%~8.67%、0.57%~6.26%、2.89%~11.16%、6.15%~30.18%、1.74%~8.46%;批间精密度分别为1.60%~6.96%、2.66%~4.72%、6.06%~15.83%、6.85%~16.01%、4.31%~5.56%;线性范围分别为0.7~4 577、4.6~12 638、1.63~70.9、1.42~17.5、9.5~22 322个/μL,线性相关系数(
UF-1000i的5个定量分析参数的批内精密度、批间精密度、携带污染率、线性范围、不准确度等指标与厂商的说明书性能相符合;与镜检符合率方面,因规范尿液离心镜检目测法不适用于尿沉渣有形成分定量,按厂商提供方法得到的符合率较高,而经
仪器投入使用前,需通过对分析系统的评价验证其性能能达到设备说明书的性能要求(制造商规定的性能要求需满足临床需要)[ 1],这是ISO15189医学实验室认可标准的要求。我们参照美国临床实验室标准化协会(CLSI)发布的H56-A文件[ 2] 及UF-1000i全自动尿液有形成分分析仪(简称UF-1000i)病例研究手册[ 3]中对体液自动化检测仪器及UF-1000i的性能评价方法对UF-1000i 5个定量分析参数[白细胞(WBC)、红细胞(RBC)、上皮细胞(EC)、管型(CAST)、细菌(BACT)]的批内精密度、批间精密度、携带污染率、线性范围、不准确度、与镜检符合率等性能进行了评价。
2009年6月至7月中山大学附属中山医院的住院和门诊患者及健康体检者的尿液标本。
Sysmex公司生产的UF-1000i及其配套试剂、质控物、校准物。
1.批内精密度 收集患者尿液标本,各参数(WBC、RBC、EC、CAST、BACT)选择高值、中值、低值3个浓度标本分别用手动进样模式和自动进样模式连续测定11次,删除第1次结果,取后10次结果分别计算差异系数( CV)值。
2.批间精密度 统计连续20 d各参数(WBC、RBC、EC、CAST、BACT)室内质控数据的 CV值。
3.携带污染率 分别取RBC、WBC、BACT高值和低值尿样各1份进行试验,先取高值样本连续检测3次,结果为H1、H2、H3;然后立即对低值样本连续检测3次,结果为L1、L2、L3,按下列公式计算携带污染率[携带污染率=(L1-L3)/(H3-L3)×100%]。
4.线性范围 (1)RBC、WBC的线性范围:取富含RBC、WBC的尿样(RBC在10 000个/μL左右、WBC在5 000个/μL左右),以鞘液作原倍、5倍、50倍、500倍、5 000倍的系列稀释后检测3次,以稀释计算值作为理论值,各稀释尿样的实测值均值与理论值进行回归统计;(2)BACT的线性范围:取富含细菌的尿样(细菌数在20 000个/μL左右),以鞘液作原倍、10、100、1 000、4 000倍的系列稀释后检测3次,以稀释计算值作为理论值,各稀释尿样的实测值均值与理论值进行回归统计;(3) EC线性范围:取高值质控液以鞘液作原倍、4、8、20、80倍系列稀释后检测3次,以稀释计算值作为理论值,各稀释尿样的实测值均值与理论值进行回归统计;(4) CAST线性范围:取高值质控液以鞘液作原倍、4、8、20倍系列稀释,以稀释计算值作为理论值,各稀释尿样的实测值均值与理论值进行回归统计;上述回归统计要求斜率值在1±0.03范围内,相关系数( r)≥0.975。
5.不准确度 统计2009年7月15日至19日共5 d WBC、RBC、EC、CAST、BACT等参数室内质控高、低值结果与SNCS(sysmex network communication system)系统中组均值的相对偏差。
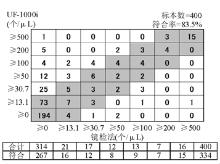
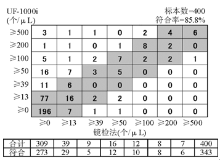
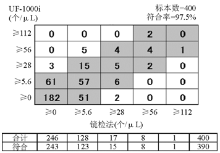
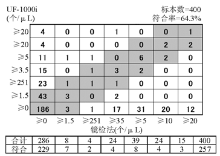
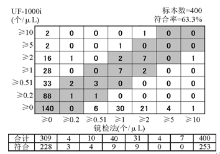
6.与镜检符合率 随机选择400例样本,含正常样本及不同程度的异常样本。样本经UF-1000i检测后,分别由2位资深检验技师用标准化的尿沉渣计数板按《全国临床检验操作规程》方法[ 4]进行镜检,镜检人员之间以双盲方法判读,根据厂商提供的统计软件,按照软件上的分级方法及符合率的判断标准统计RBC、WBC、EC、CAST、病理管型(P.CAST)的符合率,其中RBC、WBC、CAST、P.CAST计数分为7个级别,上皮细胞计数分为5个级别,分级标准见结果图。以镜检法结果为准,凡仪器检测结果与之相差一个级别的作为相互符合,计算各项目符合率。另外,根据符合率统计数据,利用SPSS13.0软件进行 Kappa检验,判断仪器检测结果与镜检法结果的一致性。
UF-1000i WBC、RBC、EC、CAST及BACT参数的批内精密度见 表1,批间精密度见 表2,线性范围见 表3,不准确度见 表4。WBC、RBC及BACT参数的携带污染率见 表5。WBC、RBC、EC、CAST、P.CAST参数与镜检符合率见 图1~ 图5,其 Kappa值分别为WBC 0.246、RBC 0.269、EC 0.291、CAST 0.018、P.CAST -0.024。
| 表1 UF-1000i 5个定量分析参数2种进样模式批内精密度[个/μL(%)] |
| 表2 UF-1000i 5个定量分析参数批间精密度[个/μL(%)] |
| 表3 UF-1000i 5个定量分析参数的线性回归方程和线性范围 |
| 表4 UF-1000i 5个定量分析参数的不准确度(%) |
| 表5 UF-1000i WBC、RBC、BACT参数携带污染率(%) |
UF-1000i基于流式细胞计数原理分析尿样中的5个有形成份,包括RBC、WBC、EC、CAST和BACT,并可定量显示。
由实验结果可见上述5个定量分析参数的批内精密度、批间精密度、携带污染率、线性范围、不准确度等方面的性能均与厂商声称的相符合。因考虑到手动进样模式与自动进样模式吸样阶段管路不同,故对上述参数的自动进样模式及手动进样模式批内精密度进行了评价,结果表明手动进样模式与自动进样模式的批内精密度基本一致。对于携带污染率方面,仪器说明书只对RBC及BACT的判断标准作了说明,本研究以RBC的标准对WBC携带污染率进行评价,结果理想。对于线性范围评价方面,对RBC、WBC、BACT的线性范围评价选择各参数高值的尿液标本以鞘液作系列稀释进行评价,因收集高浓度CAST及高浓度EC尿液标本难度高,故选择这2个参数的高值质控液用鞘液作系列稀释后进行评价;因高值质控液中EC及CAST的值比仪器声称的线性范围上限低,故证实的线性范围比仪器厂商声称的低。另外该仪器配备了参加SNCS室内质控数据实时网络比对的功能,因此通过该方法可以对仪器检测结果的不准确度进行监测[ 5]。
与镜检的符合率方面,按厂商提供的判断方法得出RBC、WBC、EC的符合率均在80%以上,CAST及P.CAST的符合率为60%以上,相关性良好。根据上述符合率数据,本研究对RBC、WBC、EC、CAST及P.CAST等5个参数的仪器检测结果与镜检法检测结果进行 Kappa检验,发现其 Kappa值均小于0.4,一致性较差,比按厂商提供的符合率判断方法得出的符合率低。因为 Kappa检验的一致性是要求两方法检测结果在同一级别才算作一致,而厂商提供的符合率判断方法为相差一个级别为符合。 Kappa值偏低也与离心镜检法的方法局限性有关,丛玉隆等[ 6]的研究发现离心法检测结果比理论值明显减少,提出规范尿液离心检查法因存在诸多影响因素,不适用于定量分析。
在研究中发现,下列因素可使检测结果偏高:(1)扁平上皮细胞及黏液丝会影响管型计数,使其假性升高,这是导致CAST及P.CAST符合率较低的原因;(2)草酸钙(特别是椭圆形草酸钙)、酵母样细胞可影响RBC的计数[ 7];大量细菌成堆出现时,与RBC相似的菌团也可误认为RBC;(3)小圆上皮细胞误认为WBC。由此可见,UF-1000i分析细胞仍存在局限性,尚不能完全代替人工镜检,须制定复检规则证实计数结果。目前对于该仪器的复检规则国内尚无统一的标准,各实验室应根据实际情况建立复检标准。只有通过制定合理的复检标准并严格执行才能保证UF-1000i检测结果的准确性。
综上所述,UF-1000i具有精密度好、线性范围广、准确度高、携带污染率低等优点,可应用于临床。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|