通讯作者:李智,联系电话:021-66306813。
作者简介:何春燕,女,1975年生,主管技师,主要从事临床检验工作。
确立、验证Sysmex XE-2100全自动血液分析仪(简称XE-2100)白细胞(WBC)高、低值的最佳复检范围。
方法将WBC<4.0×109/L及WBC>18×109/L的663例非血液病住院患者的样本分为2组,即高值组和低值组。其中高值组又分为A组(18.00~22.00×109/L,共148份)、B组(22.01~30.00×109/L,共164份);C组(>30.00×109/L,共74份)。低值组分为A'组(1.00~2.00×109/L,共90份);B'组(2.01~3.00×109/L,共92份);C'组(3.01~4.00×109/L,共95份)。对上述各组进行检测分析,以中华人民共和国卫生行业标准——白细胞分类计数参考方法为标准,通过受试者工作特征(ROC) curve曲线找出仪器检测WBC最佳复检范围,并对其进行验证。
结果A组ROC曲线下面积为0.820,当WBC为21.05×109/L时其灵敏度为1.0、特异度为0.536。B组曲线下面积为0.749,C组曲线下面积为0.329。A'组曲线下面积为0.689,B'组曲线下面积为0.825,当WBC为2.45×109/L时其灵敏度为1.0、特异度为0.317。C'组曲线下面积为0.983。验证结果:当WBC在2.45×109/L时无仪器警示标志的共28例,其中2例为假阴性,均为嗜碱粒细胞>2,无重要临床意义;有警示标志的7例,其中1例为假阳性。当WBC为21.0×109/L时无仪器警示标志的共33例,其中只有1例假阴性也是嗜碱粒细胞>2,有警示标志的7例其中3例为假阳性。
结论XE-2100的警示系统可以为复片提供有价值的信息,但血细胞计数范围的高低值也是不容忽略的复检因素。XE-2100在WBC<2.50×109/L 及WBC>21.00×109/L时分类误差较大,即便无警示标志的出现依然需进行血细胞显微镜复检,以免造成漏诊。
To establish and validate re-examination optimized range of white blood cell (WBC) high and low values of automatic hematology analyzer Sysmex XE-2100(XE-2100).
Methods663 samples of WBC <4.0×109/L (low value group) and WBC>18×109/L (high value group) were enrolled from routine inpatients without hematology disease. The high value group was further classified into A:18.00-22.00×109/L(
The area under the curve of A group was 0.820, the sensitivity was 1.0, and the specificity was 0.536 at the WBC value = 21.05×109/L. The areas under the curve of B and C groups were 0.749 and 0.329. The areas under the curve of A' and B' groups were 0.689 and 0.825. The sensitivity was 1.0,and the specificity was 0.317 at the WBC value = 2.45×109/L. The area under the curve of C' group was 0.983. The validating results showed that there were 28 samples without showing warning at WBC value = 2.45×109/L,among which 2 cases were false negative and basophilic cells>2 without clinical importance. 7 samples showed warning, and one of them was false positive. There were 33 samples without showing warning at WBC value = 21.0×109/L,among which 1 was false negative and basophilic cells>2. 7 samples showed warning,and 3 samples were false positive.
ConclusionsThe warning system of XE-2100 provides useful information for re-examination. The high and low values of WBC counting are the factors for re-examination. The error of WBC classification by instrument is large, when WBC<2.50×109/L and WBC>21×10.009/L. Microscopic examination even without any warnings is needed.
近年来,随着全自动血液分析仪的普遍运用,工作效率得到有效提高[ 1],但先进的仪器不可能完全把细胞形态分清楚,特别对特殊的细胞形态(如幼稚细胞、异型淋巴细胞、有核红细胞等),因此仪器不能完全代替显微镜的血细胞形态检查[ 2]。怎样既能保证检验准确度又能减少复检率一直是探讨的热点问题。Sysmex XE-2100全自动血液分析仪(简称XE-2100)采用的半导体激光流式原理结合细胞化学荧光染色技术,能对原始粒细胞、未成熟粒细胞、核左移、异型淋巴细胞、有核红细胞等进行报警提示。若制定合理的复片规则,通过对细胞形态复查则能补充仪器形态学的不足。由于目前各医院实验室制定的复检规则中在针对白细胞(WBC)数值各不相同,在低值方面有2.5×109/L、3.0×109/L、4.0×109/L,在高值方面有20×109/L、25×109/L、30×109/L等多种[ 3~ 5]。我们针对WBC>18×109/L及WBC<4.0×109/L的样本以手工分类为标准,对仪器分类的准确性作一评价,寻求合适的白细胞计数范围的复检规则。
选择同济大学附属第十人民医院2010年5月至10月住院(小儿科、血液病除外)患者血常规样本,共663例(其中WBC< 4.0×109/L 277份,WBC>18×109/L 386份)。用广州阳普医疗科技股份有限公司提供的乙二胺四乙酸二钾(EDTA-K2)真空抗凝管采集。
日本Sysmex公司的XE-2100流水线,由1台XE-2100及SP-1000i全自动制片染色仪组成,所用试剂均为Sysmex公司原装配套试剂,染液为BASO吉姆萨染液A液(主要成分:曙红、甲醇和亚甲蓝)、B液(缓冲液)。该仪器经SCS-1000原装配套校准品校准,参加上海市临床检验中心室内质控及室间质评,且全部在控。Nikon YS100双目光学显微镜,用于血涂片显微镜分析。
1.分组 将样本分为6组。高值组分为A组18.00~22.00×109/L,共148份,其中男83份、女65份;B组22.01~30.00×109/L,共164份,其中男86份、女78份;C组>30.00×109/L,共74份,其中男45份、女29份。低值组分为A'组1.00~2.00×109/L,共90份,其中男42份、女48份;B'组2.01~3.00×109/L,共92份,其中男35份、女57份;C'组3.01~4.00×109/L,共95份,其中男46份、女49份。
2. 仪器检测 严格按照仪器操作规程要求对样本进行血细胞分析检测,挑选出WBC<4.00×109/L,及WBC>18.00×109/L的样本,推片机推片染色,所有操作在4 h内检测完毕。
3. 显微镜镜检法 每份样本推血片2张,分别在油镜下计数200个WBC,得出各类细胞所占比值。WBC分类计数参照美国临床实验室标准化委员会(NCCLS)H20-A文件[ 6]规定的方法进行,由2名富有经验的主管技师采用双盲法,独立对血涂片进行分类。
4、验证方法 对于选定范围结果的假阴性率及假阳性率进行分析,是否漏掉对临床诊断造成影响的信息。
1.应用所检测的663份样本中仪器的警示标志,将其与手工镜检结果做比较,对警示标志的敏感度和特异度做评估,并分组进行比较。 XE-2100出现任何一项提示为阳性:(1)IG(未成熟粒细胞);(2) Blasts(原始细胞);(3)Abn Lymph/L-Blasts(异常淋巴/原始淋巴);(4)Atypical Ly(异型淋巴细胞);(5) Left Shift(核左移);(6)仅分一类;(7)不分类。其中仪器出现的重要旗标包括(1)和(2)。显微镜分类观察血涂片符合下列标准之一为阳性:(1)原始或幼稚细胞>1%;(2)晚幼粒或更早阶段细胞>1%;(3)中性杆状粒细胞>5% ;(4)异型淋巴细胞>5%;(5)浆细胞>1%;(6)嗜碱粒细胞>2 。
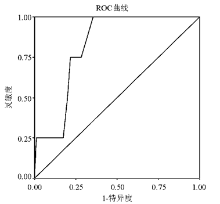
2.使用SPSS11.5统计软件,以手工分类为标准,分别对WBC<4.0×109/L及WBC>18×109/L做受试者工作特征(ROC)曲线,计算曲线下面积,了解若以WBC数值作为复核标准时的准确性。以灵敏度为纵坐标代表真阳性率,1-特异性为横坐标代表假阳性率(一般情况下,曲线下面积为0.5~0.7时,表示诊断准确性较低;面积为0.7~0.9时,表示诊断准确性中等;面积>0.9时,诊断准确性较高),试选取灵敏度较高,特异性适中的点作为复核的临界点。
| 表1 663例样本分组比较结果 |
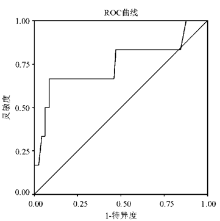
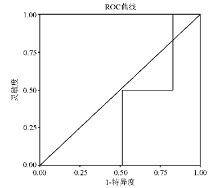
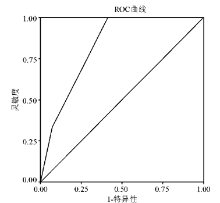
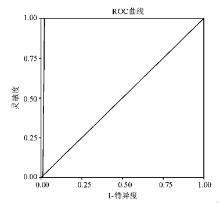
高值A组ROC曲线下面积为0.820,见 图1。其值在21.05×109/L时灵敏度为1.0、特异度为0.564,可作为高值分类的截点,具体坐标值见 表2。B组ROC曲线下面积为0.749,见 图2。C组ROC曲线下面积仅为0.329,见 图3。
| 表2 WBC为18~22×109/L时的ROC曲线指标 |
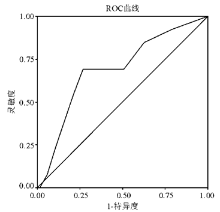
低值A'组ROC曲线下面积为0.689,见 图4。B'组ROC曲线下面积为0.825,见 图5。其值在2.45×109/L时灵敏度为1.0、特异度为0.317,可作为低值分类的截点,具体坐标值见 表3。C'组ROC曲线下面积为0.983,见 图6。
| 表3 WBC为2.00~3.00×109/L时的ROC曲线指标 |
XE-2100旗标率及手工镜检阳性率见 表4。在WBC为2.50×109/L的测定点(共35例)时无仪器警示标志的共28例,其中2例为假阴性,均为嗜碱性粒细胞>2,有警示标志的共7例,其中1例为假阳性;在WBC为21×109/L的测定点(共40例)时无仪器警示标志的共33例,其中1例为假阴性是嗜碱粒细胞>2,有警示标志的共7例,其中3例为假阳性。
| 表4 663例WBC高、值仪器旗标率及手工镜检阳性率结果 |
验证WBC在2.50~4.00×109/L中无仪器警示标志共113份,镜检阳性仅3份,为嗜碱性粒细胞>2,并无重要临床意义。在WBC为18.00~21.00×109/L中无仪器警示标志的共62份,镜检阳性为2份,1份为嗜碱性粒细胞>2,1份为杆状核>5,也无重要的临床意义。
XE-2100应用专用的WBC/BASO和WBC DIFF检测通道、半导体激光流式细胞原理结合细胞化学荧光染色技术对血液进行检测,可得到细胞散射图(X轴表示侧向散射光的强度,Y轴表示前向散射光的强度)和直方图。血液分析仪用一束半导体激光照射样本,并依据各血细胞特点产生结果,前向散射光反映细胞体积,侧向散射光反映细胞内涵物,如胞浆核颗粒,侧向荧光反映细胞DNA和RNA含量,从而保证了WBC分类的质量。但是仪器对复杂的、不典型的细胞形态识别有限,会造成一定的漏检或误判。血涂片显微镜复检能弥补仪器对细胞形态观察的不足,然而若对全部样本进行分类检查虽可保证准确性但不能满足临床快速诊断的需求,如何充分利用血液分析仪的检测结果以及所提供的报警信息来筛选所需复检的样本,提高工作效率,成为许多检验工作者追求的目标[ 7]。我们科要求所有血液科血液病患者及小儿科3岁以下患者必须进行显微镜复检,因此,本研究仅针对非血液病及小儿科的患者进行分析得出的结果。
参考国际实验血液学学会(ISLH)和美国临床和实验室标准化研究所(CLSI)推荐的国际血液学实验室“4l”条血细胞复检规则[ 8],针对我们医院具体情况,结合XE-2100的性能特点,我们医院制订出符合我们医院特征的WBC复检标准:(1)仪器出现警示标志提示;(2)WBC>20.0×109/L及WBC<3.0×109/L;(3)WBC<10.0×109/L且中性粒细胞>90%;(4)WBC分类中淋巴细胞(L)>60%;(5)单核细胞(M)>15%;(6)嗜酸性粒细胞(E)>15%;(7)嗜碱性粒细胞(B)>2%。
在日常工作中我们发现第(2)条规则中的手工镜检阳性率不高,为了避免重复劳动并不造成漏检,故作此次研究。
本研究结果显示,当WBC在3.01~4.00×109/L时其敏感度为0.83、特异度为1.0、准确度为0.99,因此我们可以信赖仪器的警示标志,不必再进行手工镜检。我们在ROC曲线较好的B'组中选取这个截点。由 表3可见在WBC 2.45×109/L时,其检测灵敏度依然可达到为1.0、特异性为0.317。因此我们认为对无仪器警示标志的WBC低于2.50×109/L也应进行涂片镜检以提高阳性检出率,以免造成漏检。
由 表1可见,当WBC计数为18.00~22.00×109/L(高值)时其灵敏度为0.76、特异性为0.84、准确度为0.83。当WBC>30.00×109/L时其灵敏度为0.89、特异性为0.63、准确度为0.70。即当WBC计数越高,仪器警示标志的准确性也越差。因此在曲线下面积较好的A组中选取这个截点。由 表2可见当WBC为21.00×109/L时,其灵敏度为1.0、特异性为0.564。因此本研究认为当WBC>21.00×109/L时应进行涂片镜检以减少误诊。
当WBC升高至>21.00×109/L时,较多是因为重度感染或肿瘤患者使用升WBC的药物,极易出现杆状核等不成熟粒细胞。本研究显示仪器对其的检测的准确性较差,对此类样本无论有无警示标志的出现均应进行手工分类,不宜将复核界限再行提高,否则极易造成漏检。
综上所述,我们认为可将WBC分类复核的临界值定在2.50×109/L 及21.00×109/L处并结合其他复检规则进行显微镜复检,以提高检验效率,把时间留给真正需要涂片复检的样本。按此标准复检率由原来的11.6%减少为11.3%。从近3个月的执行情况来看,临床未发现漏检反馈。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|