作者简介:涂少华,男,1967年生,硕士,主管技师,主要从事标记免疫分析研究。
评价光激化学发光法(LICA)对乙型肝炎病毒(HBV)感染血清学标志的检测性能。
方法用乙型肝炎表面抗原(HBsAg)定值血清和质控品对LICA检测HBV感染血清学标志的试验性能进行评价;以化学发光微粒子免疫分析法(CMIA)为比较对象,对LICA 检测453例临床样本HBV感染5项血清学标志的结果进行分析。
结果LICA对HBsAg的检测下限(LLD)为0.23 ng/mL,批内的总变异系数(
LICA检测HBV感染HBsAg、抗HBs、HBeAg、抗HBe 4项血清学标志具有良好的检测性能,与CMIA有很高的符合率。
To evaluate the analytical performance of light initiated chemiluminescence assay (LICA) in detecting the serological markers of hepatitis B virus (HBV) infection.
MethodsThe analytical performance was evaluated with quantified sera and quality control materials of HBV surface antigen (HBsAg), and the methodological comparison was carried out between LICA and chemiluminescent microparticle immunoassay (CMIA) by detecting 5 serological markers of HBV infection in 453 clinical serum samples.
ResultsThe lower limit of detection (LLD) was 0.23 ng/mL in detecting HBsAg by LICA, the total within-run coefficient of variation (
The LICA possesses satisfied analytical performance in detecting HBsAg, anti-HBs, HBeAg and anti-HBe with high consistency rate compared with CMIA.
光激化学发光法(light initiated chemilumi-nescence assay,LICA)是以纳米级高分子微粒为基础的新一代化学发光技术。国内已研制成功了LICA检测设备和相关试剂,本研究对该方法检测乙型肝炎病毒(HBV)感染的血清学标志的分析性能进行分析,并与化学发光微粒子免疫分析法(chemiluminescent microparticle immunoassay,CMIA)的检测结果作比较,以评价国产LICA的检测性能。
收集453例疑似HBV感染者静脉血,分离血清待测。LICA测定HBV感染血清学标志的仪器(型号:LiCA HT高通量免疫分析仪和LiCA SP 全自动移液器)和试剂(批号:A1013)均为上海博阳生物科技有限公司产品;CMIA测定HBV感染血清学标志的仪器(型号:ARCHITECT i2000SR)和试剂[批号:乙型肝炎表面抗原(HBsAg)83317LF00,乙型肝炎表面抗体(抗HBs)82521M100,乙型肝炎e抗原(HBeAg)81364HN00,乙型肝炎e抗体(抗HBe)86507HN00,乙型肝炎核心抗体(抗HBc)85462M500]均为美国Abbott公司产品。HBsAg标准品(adr亚型)2 份,血清定值分别为0.2和1.0 ng/mL,购自中国药品生物制品检定所,HBsAg质控品(Abbott Diagnostics Division,批号:45485HN00)。
CMIA cut-off 值:HBsAg >0.05 IU/mL,抗HBs>10 mIU/mL,HBeAg >1 S/CO,抗HBe <1 S/CO,抗HBc>1 S/CO;LICA cut-off值:HBsAg>0.2 ng/mL,抗HBs>10 mIU/mL,HBeAg >1 PEIU/mL,抗HBe >2 PEIU/mL,抗HBc>5.3 PEIU/mL。
在均相条件下,将R1(内部带有染料的纳米感光微粒)、R2(内部带有发光化合物、包被有活性分子的纳米发光微粒)与待测样本进行混合。此时R1中的感光微粒和R2中的发光微粒可迅速有效地捕捉待测物质,形成免疫夹心复合物,激发光(680 nm)照射后,感光微粒中的染料被诱导激活,并释放出高能态的单线态氧,而单线态氧能被近距离(200 nm)的发光微粒所俘获。数秒后,发光微粒将释放出高能级的红光(610 nm),用光子计数器测定发射光的光子数量,并通过测量已知浓度标准品的光子数量,拟合工作曲线,则待测物质的光子数量即可精确反映其浓度。当样本不含待测物质时,则无法形成免疫复合物,单线态氧在液相中迅速衰减,无法传递至发光微粒表面,检测时则无光子产生。
1. 检测限试验及评价 利用Abbott公司提供的HBsAg标准品制备检测限试验所需的空白样本和已知浓度系列试验样本,每一浓度样本重复测定10次,得其发光值,在工作曲线上求浓度,对每一浓度样本求平均值、标准差及变异系数( CV),按文献[1]提供的方法评价试验检测下限(lower limit of detection,LLD)、生物检测限(biologic limit of detection,BLD)及功能敏感性(functional sensitivity,FS)。LLD=
2. 精密度测定 对高、低2个浓度质控血清连续检测5 d,每天2批,每批各重复5次,计算平均批内 CV。
3. 回收率测定 取博阳公司提供的HBsAg 6点定标液各200 μL,分别加入按浓度梯度编号的离心管中,0 浓度管中不加定标液;随机取一HBsAg阳性者血清用LICA测其HBsAg浓度,然后将该血清200 μL加入已知浓度的定标液离心管中,各浓度点重复测量2次,取平均值,以各点实测平均值占期望值百分数计算回收率。
4. LICA与CMIA检测HBV感染血清学标志的比较 临床453例疑似HBV感染者血清样本,分别用CMIA和LICA进行平行检测,以CMIA为比较对象,统计分析LICA与CMIA检测HBV感染5项血清学标志结果的符合率。
采用SPSS 15.0统计软件,曲线拟合采用3次样条曲线拟合,对2种方法检测HBV感染5项血清学标志的结果采用配对 χ2检验。 P<0.05为差异有统计学意义。
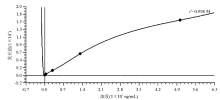
LICA共检测22批次HBsAg标准品,同一批号各点定标品的发光值连续检测5 d,每天2次。曲线拟合采用3次样条曲线拟合,取均值后的工作曲线, r2=0.998 94。见 图1。
1. 检测限及敏感性 HBsAg检测限评价试验系列标准溶液测定结果见 表1。由 表1算得,LLD=0.23 ng/mL,BLD=0.37 ng/mL,FS=0.42 ng/mL。对HBsAg敏感性标准品(adr亚型)定值为0.2、1.0 ng/mL的血清测量结果分别为0.18和1.07 ng/mL。
| 表1 HBsAg检测限评价试验系列标准溶液测定结果 |
2. 精密度 2个质控血清平均浓度分别为(10.34±0.38)和(215.32±6.32) ng/mL,低值平均批内 CV为3.67%,高值平均批内 CV为2.93%,总 CV为3.30%。
3. 回收率 不同浓度HBsAg的回收率见 表2,平均回收率为99.88%(96.10%~103.18%)。
| 表2 不同浓度HBsAg的回收率 |
在HBV感染5项血清学标志模式分析中,共有6例少见模式,1例CMIA单一HBsAg阳性而LICA阴性;2例HBsAg和抗HBs并存,2例HBeAg和抗HBe并存,2种方法结果相符;1例CMIA HBsAg阴性而HBeAg阳性,而LICA均为阴性。
LICA检测原理源于90年代问世的单线态氧分子能量传递发光免疫分析技术(luminescent oxygen channeling immunoassay, LOCI)[ 2~ 4]。该技术采用了纳米级颗粒,大大增加了生物分子的包被面积,同时借助链霉亲和素-生物素放大系统,使单位体积反应体系中含有更高浓度的生物分子,为实现超高敏感性,减少样本和试剂用量奠定了基础。另外,这种纳米颗粒在液相中保持稳定的悬浮状态,并借助于“结合则发光”原理,实现了均相、免清洗检测,和其他化学发光法相比具有如下特点:(1)LICA反应体系为均相反应,传统免疫检测技术多为非均相反应,非均相反应具有反应不充分、反应时间长、反应体系温度均一性差的缺点,而LICA整个反应是在均相中进行的,均相具有反应充分、反应时间短、反应体系温度均一性好的优点,显示出该方法具有很高的精密度;(2)LICA另一个特点是免清洗,由于在均相中反应,加上其独特的检测原理“结合则发光”,所以检测过程无须进行清洗分离,则能有效降低检测过程中的随机误差和交叉污染,最大限度地提高检测的准确度;(3)LICA样本及试剂用量微量化,每项样本及试剂用量仅25 μL,随着样本用量地大幅减少,使得检测小型化、芯片化和高通量成为可能;(4)LICA超敏感性,由于采用了纳米级微粒,增加了反应表面积,缩短了反应时间,使检测的敏感性大大提高。
HBsAg检测限试验显示,LICA对HBsAg的LLD为0.23 ng/mL,BLD为0.37 ng/mL,FS为0.42 ng/mL。博阳试剂商提供的HBsAg的LLD为0.2 ng/mL,两者的结果相近,厂商提供的敏感性是可信的。对中国药品生物制品检定所提供的HBsAg敏感性标准品检测结果,进一步验证了其敏感性的可靠性。精密度试验显示,LICA具有很高的精密度,批内总 CV<5%。同时试验具有很高的准确度,平均回收率达99.88%。本研究未对血清干扰物质进行研究,有文献报道,该方法对可能存在的干扰物质,如单线态氧淬灭物质(抗氧化剂、血红蛋白、维生素C等)、生物素结构类似物、总胆红素、三酰甘油等具有较好的耐受能力,少数物质在较高的浓度时的确存在干扰,但在常规浓度情况下,这些干扰作用可以忽略不计,表现出较高的特异性[ 5~ 7]。
以CMIA为参照,LICA对453例临床样本检测结果显示,2种检测方法对HBsAg、抗HBs、HBeAg、抗HBe的阳性率差异无统计学意义( P>0.05),而对抗HBc 2种检测方法的检出率差异存在统计学意义( P<0.01)。在最关键的HBsAg、抗HBs及HBeAg,2种方法检测结果的符合率分别为99.78%、98.45%、99.56%,具有很高的一致性。而作为辅助指标的抗HBe和抗HBc(尤其是抗HBe在某些欧美公司尚未列入测试菜单)存在一定差异,其中两者不符的样本多处于灰区、弱阳或弱阴范围。导致差异的原因是:(1)2种方法在抗HBe和抗HBc的原材料和溯源选择上存在一定差异[ 8];(2)检测原理不同,抗HBc LICA采用的是竞争法,CMIA采用的是夹心法。当2种方法检测结果发生分歧时,可寻求第三方验证,本次试验,由于样本剩余量不足,未能将所有与CMIA不符的结果进行第三方验证。此外,在HBV感染5项血清学标志少见模式分析中发现,LICA对单一HBsAg阳性和HBsAg阴性而HBeAg阳性这2种少见模式的检出能力相对不足,还有待于改进及提高。总体上,LICA与CMIA在HBV感染的血清学标志项目上符合率很高,而在个别项目上存在一定的差异,但这并不影响本评价试验得出的结论。
总之,LICA以其独特的检测技术实现了微量、敏感、快速、均相、免清洗检测,与CMIA相比,具有相近的检测性能。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|