作者简介:彭海维,女,1967年生,主管技师,主要从事临床生化及临检检验工作。
探讨采用预溶稀释血样本与全血样本检测糖化血红蛋白(HbA1c)结果的差异程度及样本放置不同时间对HbA1c测定的影响。
方法采用离子交换层析法检测全血及预溶稀释血2种样本在即刻、放置4℃ 24 h及48 h 3个时间段内的HbA1c含量并进行比较分析。比较DQ-2000全自动低压液相HbA1c检测仪(简称DQ-2000)和Rio-Rad D-10全自动高压液相HbA1c检测仪(简称HPLC)间的相对偏差。
结果DQ-2000 与HPLC的相对偏差为3.54%,全血及预溶稀释血样本精密度均在允许误差范围内,全血样本精密度稍好于预溶稀释血。全血及预溶稀释血样本保存不同时段的HbA1c浓度均低于全血即刻浓度( P<0.001)。以全血样本即刻HbA1c浓度为参比,预溶稀释血样本即刻测定HbA1c浓度的相对偏差与其余各时段比较为最小,48 h内相同时段全血样本相对偏差较预溶稀释血小,预溶稀释血及全血样本放置4 ℃ 24 h起HbA1c测定值开始下降,部分样本在放置48 h后检测结果会有所回升,但其偏差在实验室允许误差范围内。延长保存时间至72、120 h时,部分高浓度样本测定值会急剧下降,而低浓度样本测定值会明显上升,且下降与上升均无相关性,预溶稀释血样本未出现这种情况,相对较稳定。
结论采用全血样本检测HbA1c精密度较高,放置4 ℃ 48 h内稳定性较好。若样本保存时间超过48 h,采用预溶稀释血更为稳定。预溶稀释血及全血样本4 ℃保存时间越长其检测结果越低。
糖化血红蛋白(HbA1c)是血红蛋白与糖类经非酶促反应结合而生成的, 其合成缓慢且相对不可逆, 故可反映机体1~2个月内的平均血糖水平, 因此HbA1c已成为反映糖尿病患者较长时间段内血糖控制水平的良好指标[1]。目前HbA1c的测定方法主要有色谱法、电泳法、免疫法和化学法等多种, 各种方法检测结果的差异是临床关注和探讨的课题[2, 3]。DQ-2000全自动低压液相HbA1c检测仪系采用低压液相离子交换层析原理, 检测时可采用抗凝全血或预溶稀释血2种性状样本。为了解2种样本检测所产生的偏差程度以及样本放置时间对检测结果的影响, 我们对此作相关检测, 旨为临床应用提供参考。
1.对象
随机选取上海市宝山区长江路社区卫生服务中心门诊糖尿病患者32例, 男14例, 女18例, 年龄56 ~82 岁, 按文献[4]确诊。选择健康体检者38 名, 男14名, 女24名, 年龄52~88 岁。采集所有对象空腹静脉血2 mL, EDTA-K2抗凝。
2.仪器与试剂
(1)检测系统1:DQ-2000全自动低压液相HbA1c检测仪(简称DQ-2000); (2)检测系统2:Rio-Rad D-10全自动高压液相HbA1c检测仪(简称HPLC)。试剂均为原厂配套试剂。溶血剂为硼酸缓冲液。使用配套校准品对仪器进行校准。
1.样本检测
使用DQ-2000测定。将采集的70例EDTA-K2抗凝血充分混匀后根据试剂盒使用说明书要求取20 μ L全血加入980 μ L溶血剂(1∶ 50稀释)中, 待红细胞完全溶解后(5 min)混匀, 分装成3份, 其中一管与全血一同测试即刻HbA1c, 另2管与全血样本一同放入4 ℃冰箱保存(所有样本均加盖), 于24、48 h再一同取出检测HbA1c。再从中随机选取预溶稀释血及全血样本各20例延长保存时间至72、120 h进行测定。并选取正常浓度及高浓度2例样本各连续检测15次, 计算其全血样本精密度及预溶稀释血精密度。
2.相对偏差计算
选取浓度≤ 6%、6.1%~8.9%、≥ 9.0%的样本各10例, 分别使用DQ-2000(Y)及HPLC(X)进行检测, 计算2台仪器间的相对偏差[(X-Y)/Y× 100%]。
数据以 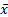
一、以HPLC测定浓度(X)为参比, 计算得DQ-2000(Y)的相对偏差为3.54%。
二、正常浓度全血样本精密度为2.52%, 高浓度全血样本精密度为1.53%, 正常浓度预溶稀释血精密度为2.54%, 高浓度预溶稀释血精密度为1.84%, HbA1c浓度越高, 检测的变异系数(CV)越小。全血样本、预溶稀释血精密度均在仪器精密度范围(< 7%)内, 全血样本精密度略好于预溶稀释血样本。
三、以全血样本即刻浓度为参比, 预溶稀释血即刻测定HbA1c浓度的相对偏差与其余各时段比较为最小, 48 h内保存相同时段全血样本的相对偏差低于预溶稀释血。预溶稀释血及全血样本放置4 ℃ 24 h起HbA1c测定值即开始下降, 其中有部分样本在放置48 h后检测结果会有所回升, 见表1、表2。
表1 全血即刻与全血保存不同时段HbA1c测定值的相对偏差(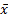 ± s, %) ± s, %) |
表2 全血即刻与预溶稀释血保存不同时段HbA1c值相对偏差(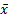 ± s, %); ± s, %); |
四、延长放置时间至72、120 h的全血及预溶稀释血样本结果
全血样本放置时间越长, 部分高浓度样本测定值会急剧下降, 而低浓度样本测定值会明显上升, 且下降与上升均无相关性, 而预溶稀释血样本未出现这种情况, 相对较稳定。见表3。
表3 全血即刻与全血及预溶稀释血样本保存72、120 h时HbA1c测定值的相对偏差(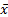 ± s, %) ± s, %) |
五、全血样本即刻检测HbA1c浓度均高于全血样本4℃保存24、48 h及预溶稀释血即刻、4℃保存24和48 h(P< 0.001), 见表4。
| 表4 全血即刻与保存不同时段HbA1c测定值的比较 |
目前临床实验室常规用于HbA1C检测的方法有两类, 第一类基于GFb和非GFb电荷的不同, 包括阳离子交换色谱法, 电泳法, 等点聚焦法等; 第二类基于GFb结构特点, 包括亲和色谱法, 免疫方法[5]。DQ-2000 和Rio-Rad D-10(HPLC)均可遡源到美国国家HbA1c标准化程序(NGSP), 本研究同批样本用DQ-2000 和Rio-Rad D-10同时检测, 以HPLC测定浓度(X)为参比, DQ-2000(Y)相对偏差为3.54%。
精密度实验中, 正常浓度及高浓度样本全血模式较预溶稀释血模式精密度高, 考虑为全血模式测试中全程自动化检测, 无人工预溶血稀释可能造成的人为误差, 其结果更加稳定。
将全血样本即刻检测的HbA1c浓度分别与全血样本4 ℃保存24 、48 h以及预溶稀释血即刻、4℃保存24、48 h测得的HbA1c浓度进行比较, 差异均有统计学意义(P< 0.001)。本研究显示预溶稀释血及全血样本4 ℃保存24 h起HbA1c浓度即开始下降, 两者部分样本在保存48 h后检测结果会有所回升。与有关报道中随着样本储存时间延长, 测定结果会逐渐升高[6]的结论相符。本研究样本4 ℃保存同样时间, 预溶血稀释样本与全血即刻的相对偏差要高于全血样本, 表明4 ℃保存48 h内全血样本的结果较预溶稀释血样本稳定。此结果与文献[7]报道的HbA1c在十四烷基三甲基溴化铵(TTAB)溶血剂中稳定时间长、检测结果稳定可靠的结论不相同。因此我们将部分样本延长保存时间至72、120 h再进行检测, 发现全血样本保存时间越长, 部分高浓度样本测定值会急剧下降, 而低浓度样本测定值会明显上升, 且下降与上升均无相关性, 而预溶稀释血样本未出现这种情况, 相对较稳定。本研究还发现部分高浓度值全血样本4 ℃保存24 h后HbA1c开始下降, 但放置48 h后又回升, 有的甚至略高于即刻值。本研究结果显示, 若样本保存时间超过48 h, 采用预溶稀释血更为稳定; 而保存时间在48 h以内则全血保存更好, 但因样本量较小(仅20例), 此结论还有待进一步论证。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|

