作者简介:黄建玲,女,1977年生,学士,主管技师,主要从事血液学检验工作。
据ISO 15189规定:当同样的检验应用不同程序或设备, 或在不同地点进行, 或以上各项均不同时, 应有确切机制以验证在整个临床适用区间内检验结果的可比性。应按适合于程序和设备特性的规定周期验证。血液分析仪由于其操作简便, 测定过程快捷, 结果准确, 精密度高, 且发展至今技术较为成熟的特点, 现已广泛应用于临床[1]。同一实验室拥有多台不同品牌, 不同型号的血液分析仪已经是普遍现象, 但是在同一实验室内不同仪器间系统误差过大, 将使检测结果失去可比性, 也为临床动态观察带来困难。为了解本科室4台血液分析仪检测结果的准确性、精密度和一致性, 我们用乙二胺四乙酸二钾(EDTA-K2)[2]抗凝的新鲜全血标本对4台仪器进行比对试验, 并将不同仪器的比对结果制作成动态分析质量图以供实验室内部质量控制。
1.仪器 Sysmex公司生产的XE-2100与 K-4500各1台; Beckman-Coulter公司生产的Coulter Ac.t diff和Beckman-Coulter Ac.t 5diff各1台。依次编号为仪器A、B、C、D。
2.试剂 使用各台仪器配套的稀释液、溶血素、鞘液、清洁液、质控品等。
3.校准品 XE-2100 使用校准物名称为SCS-1000, 校准物批号为62410525。
4.新鲜全血校准品 EDTA-K2抗凝的新鲜全血。
1.新鲜血标本的制备 取用EDTA-K2抗凝的正常体检标本若干份, 将相同血型的标本分别混合成约5 mL每管的混匀全血, 共7份。于显微镜下观察均无凝集, 分别标记为全血1~7号备用。
2.比对仪器的确定 本科室Sysmex公司的XE-2100, 使用的是可溯源的原装试剂、校准品和质控品, 定期校正, 并参加全国室间质评成绩优秀。确定XE-2100为比对仪器, 其他为测试仪器。
3.对比对仪器进行精密度检查 用全血1、2、3、4在A、B、C、D 4台仪器上连续测定11次, 去掉第1次结果, 计算白细胞(WBC)、红细胞(RBC)、血红蛋白(Hb)、红细胞平均体积(MCV)、血小板(PLT)的均数(
4.用校准物SCS-1000对XE-2100进行校准 根据中华医学会检验分会关于血液分析仪校准规范化的建议要求来判断。当各项参数
5.以仪器A为比对仪器, 用全血5、6、7分别对测定仪器B、C、D进行比对试验 全血在相应的仪器上测定11次后去掉第1次结果, 计算WBC、RBC、Hb、MCV、PLT的
6.L-J质量控制图的绘制 每日随机选择3个合格标本进行比对试验, 按上法计算出平均差异百分率, 设定靶值为0.00%, 以CLIA '88允许误差范围的1/4为差异百分率控制界限, 观察各仪器间是否存在偶然或系统误差。
用20份随机病房患者标本分别在仪器A、B、C、D上测定, 对仪器A、B、C、D测定结果作相关分析和配对t检验。统计学工具采用SPSS 11.5软件。
参比仪器与测定仪器各参数测定的差异百分率调整系数及调整后差异百分率见表1~3。调整后的差异百分率均落于允许范围内。
| 表1 XE-2100与K-4500 CV值及偏差表 |
| 表2 XE-2100与 Ac.t diff CV值及偏差表 |
| 表3 XE-2100与Ac.t 5diff CV值及偏差表 |
用20份随机病房患者标本分别在仪器A、B、C、D上测定所得数据统计分析, 求得r和P值, 结果见表4。
| 表4 XE-2100与其余3台仪器配对t检验和相关性比较结果 |
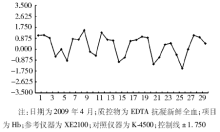
以血液分析仪K-4500为例, 血液分析仪Hb测定的比对质量控制图见图1。
随着医学检验领域的飞速发展, 现今新理论新技术不断涌现, 并很快地广泛应用于临床, 其中尤以血液分析仪的迅猛发展为突出。检测项目由过去的二分类发展至三分类到五分类。检测技术由单纯的电阻抗法发展到流式激光技术、电阻抗技术和射频技术及细胞化学技术联合使用。目前各大医院内基本都会存在不同时期购买的不同型号、不同功能的血液分析仪同时使用的现象。虽然他们都使用各自配套的全血质控物去监测仪器的精密度, 但是一般情况下同一标本在同一实验室不同型号仪器上分析, 结果可以出现不同程度的偏差。因而这会给临床带来数据的动态监测及结果解释的困难。因此有赖溯源体系的建立, 保证校准品的定值溯源至参考方法, 既可使检测结果准确, 又可使不同检测原理的分析仪在不同时间、地点得出的结果具有可比性[5]。
4台仪器的精密度均可达到厂家要求。XE-2100为参加卫生部室间质评的惟一仪器, 并参加Sysmex全球质控, 可溯源至标准参考方法。通过采用新鲜全血在4台仪器上进行比对分析的结果见表1~3。初次测量共有15个差异百分率, 其中在可接受范围的只有2个, 占总差异百分率个数的13.3%。说明3台仪器与比对仪器之间有系统误差存在, 需要校正系数校准。校准后的仪器通过新鲜全血的重新评价, 所有仪器的5个评价项目共15个差异百分率均在可接受的范围内, 说明校准是有意义以及合理的。结合表4可见, 校准后比对仪器与其余仪器各评价项目WBC、RBC、Hb、PLT及MCV的结果进行配对t检验和相关性比较, P均> 0.05, r> 0.95。因此, 不同仪器同一检查项目的检测结果差异无统计学意义, 并具有良好的相关性, 而且这种相关更具有临床意义。
新鲜全血是最佳的比对试验标本及校准物[6]。确立了本实验室的标准参比仪器后, 再利用新鲜全血建立不同品牌、不同型号的血液分析仪间的比对室内质控图, 并按照L-J质控规则对图进行分析判断, 可便于发现仪器间的偶然误差和系统误差。而且新鲜全血方便易得, 因此我们认为新鲜全血作为校准品用于血液分析仪比对试验及比对室内质控系统建立是非常有价值的。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|