作者简介:范华杰,男,1980年生,学士,技师,主要从事临床免疫学检测工作。
对Roche降钙素原(PCT)电化学发光法定量检测试剂盒(简称Roche试剂盒)进行性能评估。
方法以Biomérieux化学发光PCT试剂盒(简称Biomérieux试剂盒)为参比试剂,同时用2种试剂盒测定212例患者样本。分别以0.5和2.0 μg/L为Cut-off值进行定性统计分析;并分析2种试剂盒测定值的相关性、偏倚以及脂血、溶血、类风湿因子(RF)等对检测结果的干扰。
结果在0.5和2.0 μg/L 这2个医学决定水平,Roche试剂盒的相对灵敏度均>75%、相对特异性均>90%。与Biomerieux试剂盒的相对总体符合率较高,Kappa值均>0.8。Roche试剂盒与Biomérieux试剂盒的测定值具有良好的相关性,2种试剂盒测定值间线性偏倚无统计学意义,平均偏倚为1.0 μg/L,一致性界限为-4.6~6.6 μg/L。肝素抗凝血浆及一定浓度的脂血[三酰甘油(TG)≤18.29 mmol/L]、黄疸[总胆红素(TBil)≤541 μmol/L]、溶血[血红蛋白(Hb)≤7.6 g/L]和RF(RF≤1 380 kIU/L)对Roche试剂盒测定PCT不构成干扰。
结论Roche试剂盒在全自动电化学发光免疫检测仪上实现了PCT检测的自动化和快速化,所受干扰因素少,能完全满足临床检测需求。
降钙素原(procalcitonin, PCT)是降钙素的前体, 是由116个氨基酸组成、相对分子质量为127 000的糖蛋白。PCT由神经内分泌细胞(包括甲状腺、肺和胰腺组织细胞)表达, 经酶切分解为降钙素(CT)、羧基端肽和氨基端肽[1]。PCT在人体内的半衰期为20~24 h, 稳定性好, 在正常人血清中含量极低。
在导致全身炎性反应综合征(SIRS)的许多情况下, 诸如细菌性感染、胰腺炎、烧伤、多发伤, 血中CT前肽物质的所有剪接产物异常升高, 其中PCT是最主要的产物, 而CT则无明显变化。血PCT水平与感染及损伤的严重程度呈正相关, 且已成为用于脓毒症、严重脓毒症、脓毒症休克的诊断和疗效监测的有效指标[2]。对于社区获得性下呼吸道感染、空调诱导性肺炎以及慢性阻塞性肺疾病患者, PCT可作为抗菌药物选择及疗效判断的指标[3, 4]。PCT还可作为鉴别自身免疫性炎性反应和细菌感染炎性反应的有效指标。对于器官移植患者, 应用PCT定量检测还可以有助于鉴定是否为手术引起的继发性感染还是急性排斥反应[5]。
我们对Roche PCT电化学发光法试剂盒进行性能评估。以了解该试剂盒是否能满足临床检测需求。
采集212例第二军医大学附属长海医院住院患者血清, 其中男性143例、女性69例, 平均年龄47岁。212例样本中有61例采自血培养等病原微生物检测阳性的患者, 分离的病原微生物前4位分别为:大肠杆菌、肺炎克雷伯菌、铜绿假单胞菌、鲍曼不动杆菌。还包括溶血、肝素抗凝血浆、脂血、黄疸、类风湿因子阳性等各10例样本, 用作干扰比对试验。血清样本的收集和本次临床实验均经长海医院伦理委员会批准。
仪器为Roche cobas e 601全自动电化学发光免疫检测仪, Biomé rieux mini-VIDAS自动荧光免疫分析仪。Roche PCT电化学发光法试剂盒(简称Roche试剂盒, 批号154910-2), Biomé rieux PCT化学发光法试剂盒(简称Biomé rieux试剂盒, 批号833349501)。
1.Biomé rieux PCT化学发光法 采用双抗体夹心一步法。待检样本先与包被在固相上的抗PCT抗体结合, 在与孔中的碱性磷酸酶标记的抗PCT单克隆抗体结合; 以405 nm波长检测底物水解后产生的荧光强度反映PCT的浓度。检测线性范围为0.05 200 μ g/L, 以批间检测CV≤ 20%时得到的最低分析物浓度为0.09 μ g/L。
2.Roche PCT电化学发光法 采用双抗体夹心二步法。待检样本与生物素化的单克隆PCT抗体以及钌复合物标记的单克隆PCT抗体一起孵育, 形成抗原抗体夹心复合物。加入包被链霉亲和素的磁珠微粒, 复合物与磁珠通过生物素和链霉亲和素的作用结合。通过电磁作用将磁珠吸附在电极表面, 给电极加以一定的电压, 使复合体化学发光, 并通过光电倍增器测量发光强度。方法学的检测线性范围为0.02~100 μ g/L, 以批间检测CV≤ 20%时得到的最低分析物浓度为≤ 0.06 μ g/L。
1.相关性及偏倚分析 以Biomé rieux试剂盒作为对照检测系统考核Roche试剂盒的检测结果。2种方法学检测结果的回归分析采用Passing-Bablok回归和一元直线回归分析。偏倚分析采用Bland-Altman方法, 以2种方法测定结果的均值作为X轴、差值为Y轴。
2.计算相对灵敏度 以Biomé rieux试剂盒为参比试剂盒, 分别以0.5和2.0 μ g/L为Cut-off值, 计算Roche试剂盒的各项特异性指标。包括相对灵敏度、相对特异性、相对总体符合率。
3.干扰实验 10例脂血样本的三酰甘油(TG)浓度为1.84~18.29 mmol/L(平均为6.67 mmol/L); 10例黄疸样本的总胆红素(TBil)浓度为44.1~541 μ mol/L(平均225.46 μ mol/L); 10例类风湿因子(RF)阳性样本的RF浓度为23.4~1 380 kIU/L(平均242.68 kIU/L); 10例溶血样本的血红蛋白(Hb)浓度为3.0~7.6 g/L(平均4.8 g/L); 肝素抗凝血浆样本10例。每份样本用2种试剂盒各测定3次, 取均值。观察2种试剂盒检测结果的差异。
Passing-Bablok回归的线性检测采用Cusum法, P< 0.05表示线性回归偏倚具有统计学意义。一元直线回归分析计算相关系数(r), r> 0.975表示相关性良好。应用Kappa一致性检验判定2种试剂盒间检测定性结果的一致性, 以Kappa值≥ 0.75表示两者一致性较好、Kappa值为0.4~0.75表示两者一致性一般、Kappa值< 0.4表示两者一致性较差。
202例样本(不包括RF阳性的10例样本)以Roche试剂盒的检测结果划分浓度梯度, 其中PCT浓度为0.05~0.5 μ g/L的91例、0.5~2 μ g/L的28例、> 2 μ g/L 的43例。Roche试剂盒有27例检测结果< 0.02 μ g/L; Biomé rieux试剂盒有56例检测结果< 0.05 μ g/L。另有2例样本检测结果高于2种试剂盒的检测上限。因此, 将其中用2种试剂盒检测均获有效数据的139例样本进行相关性和偏倚分析。Roche试剂盒检测PCT的均值为3.28 μ g/L、范围为0.022~98 μ g/L; Biomé rieux试剂盒PCT的检测均值为4.27 μ g/L、范围为0.05~132 μ g/L。
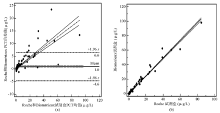
相关性分析显示Roche试剂盒的测定值与Biomé rieux试剂盒的测定值呈显著相关(回归方程为YBiomé rieux=0.273 4+1.218 6XRoche, r=0.977 3, P< 0.01)。方程斜率的95%可信区间(CI)为1.192 61.244 6; 截距的95%CI为0.000 481 10.546 4。线性回归的Cusum检验证实偏倚无统计学意义(P> 0.05)。Bland-Altman分析显示Roche试剂盒与Biomé rieux试剂盒测定值的平均偏倚为1.0 μ g/L, 一致性界限为-4.6~6.6 μ g/L, 见图1。
202例样本的测定值以0.5 μ g/L 为Cut-off值进行定性统计分析, 结果见表1。Roche试剂盒的相对灵敏度为87.2%, 相对特异性为99.2%, 与Biomé rieux试剂盒测定结果的相对总体符合率为94.6%, Kappa值为0.828。以2.0 μ g/L 为Cut-off值进行定性统计分析, 结果见表2。Roche试剂盒测定的相对灵敏度为82.2%, 相对特异性为100.0%, 与Biomé rieux试剂盒测定结果的相对总体符合率为96.0%, Kappa值为0.877。
| 表1 以0.5 μ g/L为Cut-off值进行定性统计分析结果 |
61例临床病原微生物检测阳性患者样本的测定值以0.5 μ g/L为Cut-off值进行定性统计分析。Roche试剂盒和Biomé rieux试剂盒的检测阳性率分别为62.2%和68.7%, Kappa值为0.855, 仅4例样本的检测结果不符合。如果测定值以2.0 μ g/L 为Cut-off值进行定性统计分析, Roche试剂盒和Biomé rieux试剂盒的检测阳性率分别下降为39.3%和44.2%, Kappa值为0.899。
| 表2 以2.0 μ g/L为Cut-off值进行定性统计分析结果 |
TG≤ 18.29 mmol/L、肝素抗凝血浆、TBil≤ 541 μ mol/L、Hb≤ 7.6 g/L对2种试剂盒的测定均无影响。在10例RF阳性样本中, 2种试剂盒的测定值出现明显差异, 见表3。其中有4例Biomé rieux试剂盒的测定值> 2.0 μ g/L、1例> 0.5 μ g/L; 然而, 这5例样本Roche试剂盒的测定值均≤ 0.02 μ g/L。分析这4例Biomé rieux试剂盒测定值> 2.0 μ g/L的患者的诊断和实验室检查情况, 发现这4例患者的诊断均为类风湿性关节炎, 白细胞总数和嗜中性粒细胞分类除1例偏高外, 其余均正常。
| 表3 10例类风湿因子阳性血清2种试剂盒测定PCT的结果比较 |
对细菌感染和患败血症的患者早期诊断和早期治疗是急诊室和重症监护单位的重大挑战。由于人口老化、更广泛地使用侵入性操作和免疫抑制剂的使用等原因, 使败血症的发生率和疾病严重程度增加。因败血症的临床症状和体征无特异性, 并常常与其他非感染性全身炎症重叠出现, 致使败血症的诊断困难。但是, 败血症的早期诊断和治疗是提高生存率的关键。白细胞计数、急性时相反应蛋白[以C反应蛋白(CRP)为主]、白细胞介素(IL)-6、IL-8等细胞因子的检测是传统判断及评估炎性反应的检测指标。但以上项目一直受各方面因素的制约和影响, 并已被证明在确定患者是否采取抗菌药物治疗等方面作用非常有限。
随着PCT定量检测技术的应用, PCT已成为与细菌性感染炎性反应相关的特异性指标, 特别成为快速鉴别细菌性感染所致的SIRS及脓毒症、尤其是重症脓毒症和感染性休克脓毒症休克的重要指标。对于鉴别感染与非感染所致的炎性反应(如自身免疫性炎症、移植急性排斥反应)具有重要意义。为指导临床抗菌药物的如何合理使用, 疗效评估及缩短抗菌药物的使用时间[6]带来重要的革新。同时PCT的定量检测配合微生物学检测技术有助于院内感染的快速追溯及控制。
本研究主要针对Roche试剂盒进行临床应用性能评价。由于Biomé rieux试剂盒是最早获得国家药品和食品监督管理局进口注册的产品, 故以此作为参比试剂盒进行了相关性分析。本研究证明Roche试剂盒与Biomé rieux试剂盒具有良好的相关性, 2种试剂盒测定值间线性偏倚无统计学意义; 平均偏倚为1.0 μ g/L, 一致性界限为-4.6~6.6 μ g/L。选择0.5和2.0 μ g/L 这2个医学决定水平是因为血PCT含量低于0.5 μ g/L 通常被认为排除脓毒血症, 介于0.5~2.0 μ g/L之间被认为可能脓毒血症, 高于2.0 μ g/L 则为脓毒血症或由细菌感染所致的SIRS[7, 8]。在0.5 和2.0 μ g/L这2个医学决定水平, Roche试剂盒的相对灵敏度均> 75%、相对特异性均> 90%, 与Biomé rieux试剂盒的相对总体符合率较高、Kappa值均> 0.8。本研究利用61例临床微生物检测阳性患者的血清对0.5和2.0 μ g/L 这2个医学决定水平进行了评价。以0.5 μ g/L作为Cut-off值, Roche试剂盒和Biomé rieux试剂盒的检测阳性率分别可达到62.2%和68.7%; 以2.0 μ g/L作为Cut-off值则检测的敏感性明显降低, 阳性率低于45%。因此, 本研究认为在临床中使用0.5 μ g/L作为Cut-off值比较合适, 可保证检测一定的敏感性和特异性。本研究结果还显示2种PCT定量测定试剂盒的测定值均不受肝素抗凝血浆以及一定浓度脂血、黄疸、溶血的影响, 并且Roche试剂盒的测定值亦不受一定水平RF的影响。然而, Biomérieux试剂盒在抗RF干扰的性能上似乎较弱。
随着PCT检测项目向临床的开放, 对于检测技术的准确快速和高效提出了新的要求。Roche试剂盒在全自动电化学发光免疫检测仪上实现了PCT检测的自动化和快速化, 所受干扰因素少, 能完全满足临床检测需求。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|