作者简介:郑瑾,女,1972年生,主管技师,主要从事临床免疫学检验工作。
对颗粒增强透射免疫比浊法(PETIA)测定血清半胱氨酸蛋白酶抑制剂C(Cys C)进行方法学评价。
方法根据美国临床实验室标准化委员会(NCCLS)EP5-A、EP6-A、EP9-A及EP7-P文件对PETIA测定血清Cys C的精密度、可报告范围、方法学比较及干扰实验进行评价和比较。
结果PETIA的低水平样本批内变异系数( CV)为1.34%、批间 CV为2.19%、日间 CV为1.82%、总 CV为2.56%;高水平样本批内 CV为1.15%、批间 CV为1.40%、日间 CV为2.23%、总 CV为2.58%。可报告范围为0.44~4.46 mg/L。PETIA与颗粒增强散射免疫比浊法(PENIA)呈显著相关[决定系数( r2)=0.997 2, P<0.01]。血红蛋白(Hb)<5 g/L、三酰甘油(TG)<12 mmol/L、总胆红素(TBil)<150 μmol/L 时,PETIA测定Cys C高、低水平样本的干扰值均在干扰限度值(1.96 s)范围内。
结论PENIA具有良好的重复性,与PENIA有良好的相关性,抗干扰能力较强。因此PETIA是测定血清Cys C较理想的方法,可应用于临床检测。
目前, 检测血清半胱氨酸蛋白酶抑制剂C(Cys C)的方法主要有颗粒增强散射免疫比浊法(PENIA)和颗粒增强透射免疫比浊法(PETIA)2种[1]。我们根据美国临床实验室标准化委员会(NCCLS)EP5-A(临床化学设备精密度性能的评价) [2]、EP6-A(定量分析方法线性的评价)[3]、EP9-A(方法学比较评价)[4]及EP7-P(临床化学实验干扰)[5] 文件对PETIA测定血清Cys C作出评价。
HITACHI 7600P全自动生化分析仪(简称7600P)及BN-100特定蛋白分析仪(简称BN-100)。
1. 7600P的PETIA采用北京利德曼生物技术有限公司提供的Cys C透射比浊试剂盒(批号A803D14)、定标液(批号A7H1D02)、质控品(低值和高值, 批号:A803D14)。
2. BN-100的PENIA采用Behfing公司提供的Cys C试剂(批号38663)、定标液(批号049848)及Biorad公司提供的质控品低值(批号52341)、高值(批号53343)。
收集本院住院患者及健康体检者血清样本182例, 其中男112例、女70例, 年龄21~76岁。
1. 选取无黄疸、溶血和乳糜干扰的患者样本配制2份混合血清(低水平样本为0.82 mg/L, 高水平样本为2.78 mg/L)各分成2份, 对7600P做精密度评价。
2. 选取无黄疸、溶血和乳糜干扰的严重肾病和肾功能衰竭患者的混合血清作为高值样本(H), 浓度为2.12 mg/L。健康体检者混合血清加少量蒸馏水作为低值样本(L), 浓度为0.11 mg/L。H和L样本按4L、3L+1H、2L+2H、1L+3H、4H配成系列样本, 对7600P做可报告范围评价。
3. 选取可报告范围内40例样本作为研究对象, 其浓度选择按照按NCCLS EP9-A文件中方法对比实验数据分布建议表的要求, 尽可能覆盖检测范围, 对7600P做方法学比较评价。
4. 选取精密度评价中的低水平样本(浓度为0.82 mg/L)和高水平样本(浓度为2.78 mg/L)各分成2份, 1份加入干扰物配制成干扰溶液作为测定样本(T), 另1份加同样体积的蒸馏水作为对照样本(C), 对7600P做干扰实验分析。
1.精密度评价依据EP5-A文件。取混合血清2份, 每天测定2次, 2次测定间隔不少于2 h。每次测定对样本均作双份检测, 共测定20 d。每次测定至少做1个质控。分析PETIA低水平样本与高水平样本的总不精密度[包括批内、批间、日间和总变异系数(CV)]。
2.可报告范围评价依据EP6-A文件。将样本按不同程度稀释或配置后, 将预期值与实测值比较。每个样本重复测定4次(Y1 ~Y4), 以预期值为横轴X, 实测值为纵轴Y, 用直线回归统计处理结果, 直线所达的限值即为该方法结果的可报告范围。期间必须进行组内离群点检查, 计算极差D= Y1-Y4, 分析离群点。若 Y1 可能是离群点, 则D1=(Y1-Y4)/D 。 若 Y4可能是离群点, 则 D4=(Y3-Y4)/D。计算结果( D1或D4)如果大于 0.765 (0.05) 或 0.889 (0.01) , 则该点判为离群点。依据EP6-A文件允许从分析数据中删除离群点, 再进行直线回归统计。
3.方法学比较依据EP9-A文件。以PETIA为实验方法, PENIA为比较方法, 样本测定在5个工作日每天测定8个样本, 测定时第1次按顺序1→ 8, 第2次8→ 1, 共测5 d, 分别用BN-100和7600P对每个样本进行双份平行测定。作散点图:Y轴为实验方法每样本双份测定的均值; X轴为比较方法每样本双份测定的均值。
4.分析干扰实验依据EP7-P文件。(1)溶血干扰物:取新鲜乙二胺四乙酸(EDTA)抗凝全血加蒸馏水配制, 血红蛋白(Hb)浓度分别为5、3、1 g/L; (2)三酰甘油(TG)干扰物:取高血脂患者样本加蒸馏水配制, TG浓度分别为12、6、3 mmol/L; (3)胆红素干扰物:取黄疸患者样本加蒸馏水配制, 总胆红素(TBil)浓度分别为150、100、50 μ mol/L; (4)计算:低水平样本和高水平样本各分成2份, 每份样本重复测定5次计算分析干扰值:干扰值=T-C, 即各组均值-未加干扰物相应组的均值。干扰值在对照组1.96 s(95%可信区间)范围内为无显著干扰。
采用SPSS统计软件作相应统计。以连续变量的统计描述与参数估计做精密度评估; 以直线回归分析做可报告范围评估及方法学评估。采用NCCLS评价方案EP文件应用软件做分析干扰评估。
7600P测定Cys C可报告范围评价结果, X为Cys C的预期值, Y1~Y4为Cys C 4次重复测定的实测值, 见表2。7600P测定Cys C可报告范围直线回归方程为Y=0.726 1X+0.023 3, 决定系数(r2)=0.880 9。Cys C在0.44~8.48 mg/L范围内不成线性。进行组内离群点检验, 去除8.48和 6.47 mg/L 2个浓度点后组间离散程度均小于0.05, 不影响线性判断。直线回归方程为Y=0.942 7X+0.011 9, r2=0.994 7。7600P测定Cys C可报告范围为0.44~4.46 mg/L。
| 表2 Cys C可报告范围评价的预期值和实测值(mg/L) |
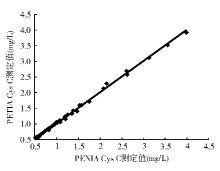
在Cys C可报告范围内PETIA与PENIA呈显著相关, 相关方程为Y=1.002X+0.005, r2=0.997 2, P< 0.01。见图1。
低水平样本(0.82 mg/L)的s批内为0.011, 计算干扰限度值(1.96 s)为0.021。高水平样本(2.78 mg/L)的s批内为0.032, 计算干扰限度值(1.96 s)为0.062。Hb< 5 g/L、TG< 12 mmol/L、TBil< 150 μ mol/L时, PETIA测定Cys C高、低水平样本的干扰值均在干扰限度值(1.96 s)范围内, 因此均不构成干扰。
血清Cys C作为一项理想的反映肾小球滤过功能的指标现已在临床上广泛使用[6]。Cys C测定方法主要基于免疫反应原理。PETIA和PENIA采用Cys C特异抗体包被胶乳或聚苯乙烯粒子做自动均相免疫分析, 容易在自动化仪器上操作, 具有简单快速的特点, 为临床检测Cys C提供了极大方便。
本研究依据NCCLS制订的评价方案, 对7600P的PETIA测定Cys C的精密度、可报告范围、方法学比较及干扰实验进行评价和比较。结果显示低水平样本批内CV为1.34%、批间CV为2.19%、日间CV为1.82%、总CV为2.56%; 高水平样本批内CV为1.15%、批间CV为1.40%、日间CV为2.23%、总CV为2.58%。可报告范围为0.44~4.46 mg/L。PETIA与PENIA呈显著相关(r2=0.997 2, P< 0.01)。Hb< 5 g/L、TG< 12 mmol/L、TBil< 150 μ mol/L时, PETIA测定Cys C高、低水平样本的干扰值均在干扰限度值(1.96 s)范围内。
本研究7600P测定Cys C的可报告范围为0.44~4.46 mg/L, 低于试剂说明书给出的线性范围(8.0 mg/L)。进行组内离群点检验, 去除8.48和 6.47 mg/L 2个浓度点后组间离散程度均小于0.05, 不影响线性判断。说明高值样本测定结果具有一定的差异, 这一点与国内外报道一致[7, 8]。分析原因, 可能是由于钩状效应的影响, 当抗原量过剩时会出现后带现象, 过量的抗原与免疫复合物结合会导致复合物的降低, 此时就需要稀释样本后重新进行测定。本研究由于未得到Cys C纯品, 不能制备> 8.0 mg/L的Cys C溶液, 所以无法评价高浓度样本的检测结果。因此在遇到高值样本时, 需稀释一定倍数后再进行检测, 以保证结果的准确性。
由此可见在对PETIA进行精密度评估后, 证明批内批间具有良好的重复性。北京利德曼生物技术有限公司提供的Cys C透射比浊试剂线性范围是0~8 mg/L, 但我们在实验室检测结果的最大范围是0.44~4.46 mg/L, 在> 4.46 mg/L的情况下精密度、准确度等不能满足要求。因此将可报告范围下调至4.46 mg/L。方法学比较后, 证明PETIA和PENIA 2种方法有良好的直线相关。分析干扰实验后, 在PETIA测定Cys C可报告范围(0.44~4.46 mg/L)内Hb< 5 g/L、TG< 12 mmol/L、TBil< 150 μ mol/L时PETIA测定Cys C高、低水平样本均不构成干扰。因此PETIA是测定Cys C较理想的方法。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|