作者简介:柯培锋,男,1979年生,医学硕士,主管技师,主要从事临床生物化学检验、临床实验室质量管理及实验室认可工作。
甲状腺疾病是内分泌疾病中最常见的疾病之一,美国国家临床生物化学协会以促甲状腺激素(TSH)检测为中心的策略评价甲状腺功能[ 1]。将TSH作为一线检测项目,根据TSH的检测结果是否异常,再检测游离甲状腺激素(FT4),对甲状腺疾病进行鉴别诊断。在甲状腺功能亢进临床分型中的轻度、亚临床型甲状腺功能亢进及非甲状腺疾病(NTI)者出现一过性的TSH异常,TSH通常在0.01~0.1 μIU/mL,此时只有TSH才能检测到轻度、亚临床甲状腺功能异常[ 2]。SIEMEMS Centaur 240全自动分析仪检测TSH是采用双抗体夹心化学发光法,厂家给出的TSH最低检测浓度为0.01 μIU/mL。为得到本实验室TSH的检测限值和定量限值, 建立适合本实验室低值TSH定量报告的模式,进行了本实验。
1. 检测仪器、试剂 德国SIEMEMS Centaur 240全自动化学发光分析仪。TSH定量检测试剂由主要试剂(含磁性微粒的固相抗原或抗体,标记的抗原或抗体)、稀释液、发光试剂组成,均由德国西门子公司提供的原装配套试剂,批号:001213。
2. 样本 收集20例广东省中医院门诊和住院患者TSH检测浓度为0 μIU/mL的新鲜混合血清作为空白样本,混匀后分装成30管,-20 ℃冰箱保存备用。收集20例广东省中医院门诊和住院患者TSH检测为低浓度0.1 μIU/mL的新鲜混合血清,重复检测5次,去除最高值和最低值计算其均值为该血清的TSH浓度值,用稀释液作系列稀释,组成预测值为0.01、0.02、0.025、0.03、0.035、0.04 μIU/mL 的系列低水平检测样本,分装成30管,依次编号为C1、C2、C3、C4、C5、C6,4 ℃冰箱保存备用。
3. 空白限值[ 3] 每天检测6管空白样本,上、下午各检测1次,连续5 d,共得60个空白结果。按α=β=5%,空白限值(LoB)=μB+1.645σB。α代表 Ⅰ 型错误/假阳性;β代表II型错误/假阴性,式中μB、σB分别代表空白检测的均数和标准差。
4. 检出限值[ 3] 各浓度样本每天上、下午各测1次,连续5d,共得60个低水平样本结果。若数据呈正态分布,则LoDST=LoB+Cβ SDs, Cβ=1.645/[1-1/(4*f), SDs为低水平样本精密度的综合估计值,即 SDs2=(n1 SDs12+n2 SDs12+...nn SDsn2)/(n1+n2+...+nn),其中n1=N1-1,n2=N2-1,N1、N2……Nn为各个样本的重复检测数;Cβ是标准正态分布的第95百分位数(纠正因子);f是估计标准差SDs自由度。若数据呈非正态分布,则用非参数统计,计算检出限值(LoD)。
5. 定量限值[ 3] 计算6个低水平样本的日间不精密度( SD)、实测值(均值)和预期值的偏差以及总误差(TE),TE=偏差+2 SD,若TE<CLIA'88TEa,则定量限值(LoQ)=LoD,否则需选择更高浓度的低水平样本重新进行检测。
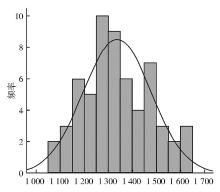
1.计算LoB 对60个空白样本的检测值( 图1)按光强度值(RLU)进行正态性检验,结果显示该组数据呈正态分布,可按公式LoB=μb+1.645*σb计算,均值为1 336.5,标准差为140.887,LoB=1 568.26。按浓度进行正态性检验,结果为非正态分布,用非参数估计第95%百分数所在位置:[NB(95/100)+0.5]的值, Nb=60,则第95%百分位数应该是第57与第58个观察值的均值,即LoB= 0.01 μIU/mL。
2. 计算LoD 低浓度患者混合血清重复检测5次的TSH浓度为0.1、0.09、0.1、0.09、0.1 μIU/mL,根据其RLU去除最高值和最低值后计算平均值为0.096 7 μIU/mL。系列低水平检测样本,结果见 表1。
| 表1 系列低水平检测样本的浓度和RLU(μIU/mL) |
对各组数据进行正态性检验,结果不全是正态分布。
采用K个相关样本Friedman检验,检验各低水平样本的标准差是否恒定。结果显示,Chi-Square统计量为31.275,自由度为5,各低水平样本间的差异均有统计学意义( P<0.01)。对数据进行非参数统计,即将数据从大到小排列,计算β-百分位数, LoD是β=5%处的结果。第5%百分数所在的位置是[ND(5/100)+0.5]的值,式中ND为检测次数,ND=60,则第5%百分位数应该是第3与第4个观察值的均值,LoD=1 641.5(RLU),LoD=0.02 μIU/mL。
3. 计算LoQ 计算6个低水平样本的日间SD、均值和预期值的偏差以及TE,TE=偏差+2SD,经计算得TE=0.020 1,目标设定CLIA'88TEa规定TSH的允许范围是“靶值±25%”,TE<CLIA'88TEa,则LoQ=LoD 0.02 μIU/mL。
高灵敏度的TSH检测可用于甲状腺功能亢进和亚临床甲状腺功能亢进的诊断。明显甲状腺功能亢进时TSH在0.01 μIU/mL以下,而在轻度、亚临床甲状腺功能亢进时以及NTI时,TSH受抑制较轻,一般在0.01~0.1 μIU/mL,此时可结合FT4来判断甲状腺功能[ 2]。
美国临床与实验室标准学会(CLSI)于2004年发布了EP-17A文件[ 4]——确定检出限值与定量限值的方案。空白限值[ 3]是指(在规定的可能性条件下)空白样本被观察到的最大检测结果。LoB不是检测得到的实际浓度,而是确保在实际浓度处观察到的检测结果,其是在规定的可能性条件下,含有分析物等于LoD水平的样本预期得到的最低值。在LoB的计算中引入了国际标准化组织(ISO)推荐的“在规定水平的Ⅰ类错误与Ⅱ类错误下确定最小检出限值”,常默认为α=β=5%,相比计算分析灵敏度中的检测低限的“2 SD”要小。在本实验中,选择的患者血清是在该批号低浓度(0 μIU/mL)标准液的RLU(1391)附近的“0” μIU/mL血清,与常规样本的基质相差较小。对于小部分测出为0.01 μIU/mL的数据,除了反复冻融引起纤维蛋白析出的可能外,更主要的原因是测试过程中仪器本身和环境以及操作者的因素对低浓度样本影响较大。检出限值[ 3]是指在规定的可能性条件下予以检出的样本中分析物的最小值。也被称为“检出低限”、“最小的可检出的浓度”,有时候用于指示“灵敏度” 。LoD是最低的可靠检出的实际浓度,在该浓度处观察的检测结果非常有可能超过LoB,但还不能量化。在本实验中,结果在0.01 μIU/mL~0.02 μIU/mL的样本就被认为95%的可能性>空白,相当于阳性样本,但还不能定量报告。在对系列低水平样本的数据进行Friedman检测的结果显示,各低水平的标准差是有差异的,说明反应或者样本的不稳定影响了变异,这可能是由于选用的稀释液和低浓度新鲜血清存在的不稳定因素所造成。定量限值[ 3]是指样本中分析物的最小量,在规定的可接受精密度和正确度下被定量地确定。也被称为“确定低限”和“检测范围的低限”。LoQ可略>或等于LoD。在本实验,LoQ=0.02 μIU/mL,厂家声明“最低检测浓度0.01 μIU/mL”,所用样本仅为空白样本,相当于LoB,与本实验结果相符。另外,在低值样本的选择中存在偏差,相比标准液患者血清没有溯源性,不正确度较大,最终影响LoQ的确定。但生物检测限和功能灵敏度的计算中,没有涉及到不正确度,只包含精密度,这同样让人怀疑其可靠性。
与国际纯品和化学联合会(IUPAC)定义的“分析灵敏度”相比较,EP-17A方案还有以下特点:(1)不需要数据符合正态分布,可运用非参数统计,更适用于实际;(2)不要求标准差是恒定的,而在分析灵敏度的计算中已默认系列检测限的标准差是相同的。前两点会造成计算出来的限值比EP-17A的要小;(3)不需要知道分析物的原始值,实验中分别计算RLU和浓度值的均值、标准差来确定LoB和LoD,结果是相符的,而计算生物检测限和功能灵敏度时则需要用原始值减去空白样本的原始值使检测起点为0,再进行浓度转换。该方案还以检验的允许误差来估计定量限值,充分保证了检验结果即使在低值条件下也能符合临床需求质量管理要求[ 3]。
本实验结果,凡低于0.02 μIU/mL的结果都不能定量报告;TSH≤0.01μIU/mL,则报告“TSH<0.02 μIU/mL”或“不能检出”;若TSH≥0.02 μIU/mL,则直接报告检测值。而在日常工作中,检测结果为 “0”或是浓度<0.02 μIU/mL等的结果也不少,此时可以根据我们的实验结果进行更加科学的报告。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|