作者简介:王高生,男,1958年生,主管技师,主要从事临床免疫工作。
研制化学发光免疫分析法(CLIA)癌胚抗原 (CEA)检测试剂盒。
方法采用双抗体夹心法用2种不同的单克隆抗体分别与CEA分子上不同的抗原决定簇发生反应。用1株单抗包被微孔板制成固相抗体,用另1株单抗标记碱性磷酸酶(ALP)制成酶标抗体。在包被微孔中加入CEA校准品或待测血清及酶标抗体,温育后即形成固相抗体-抗原-酶标抗体的复合物,充分洗涤后加入化学发光底物液,于30~90 min内测定其发光强度(RLU),根据标准曲线即可算出标本中CEA的含量。
结果该试剂盒其敏感性可达0.058 ng/mL;批内和批间变异系数( CV)分别为5.5%~9.3%和10.2%~12.2%。经实验表明,CLIA与免疫放射分析法(IRMA)和酶联免疫吸附试验(ELISA)分别呈高度相关,相关系数( r)分别为0.991、0.984;平均回收率为97.3%。
结论新研制的CEA CLIA试剂盒各项技术指标均达到了国外同类产品水平。
癌胚抗原(CEA)是目前国际上公认的一种肿瘤标志物。检测CEA的含量有助于恶性肿瘤的临床诊断, 是病程进展、治疗效果、预后、复发、转移等的一个很好的监测指标[1]。近几年国内也在逐步开始化学发光免疫分析法(CLIA)的研究, 基本处于刚起步阶段, 还没能很好地解决固相抗体的包被技术(常规的包被方法依靠物理吸附, 包被板变异大, 包被抗体易脱落)、酶的标记工艺(过去的标记方法步骤较多, 酶和抗体易失活)和高效稳定的化学发光底物液, 这也是国内酶联免疫吸附试验(ELISA)仅限于定性分析, 没能向定量分析发展的原因[2]。我们经过几年的研究创新, 已经突破了这些关键技术, 现就此项技术进行总结分析。
CEA纯品为北京北免东雅生物技术研究所提供; CEA单克隆抗体购自北京生物制品研究所; 碱性磷酸酶(ALP)购自Sigma公司; 化学发光剂购自PE公司; 酶联微孔板购自Corning Costar公司。BHP9504型微孔板发光分析仪为滨松光子有限公司生产。
1. 原理 用高活性的ALP标记抗体, 以环化1, 2-二氧乙烷的衍生物(AMPPD)及增强液为发光底物。CLIA原理是AMPPD在ALP作用下, 分子上的磷酸酯键部位水解, 脱去1个磷酸基, 生成1个中等稳定的中间体2-氨基-2甲基-1-丙醇(AMPD)。AMPD经自身内电子转移裂解为一分子的金钢烷酮和一分子处于激发态的间氧苯甲酸甲酯阴离子, 当其回到基态时发出470 nm的光, 再通过发光分析仪来检测其光信号。
2. 抗体包被板的制备 取CEA单克隆包被抗体, 用pH值4.8的0.05 mol/L柠檬酸缓冲液配制成抗体浓度为10 μ g/mL的包被液, 再加入一定量的交联剂, 分别加到发光微孔板中, 每孔110 μ L, 室温放置3 h, 然后4 ℃放置24 h, 用生理盐水洗3次后, 每孔加封闭液[0.5%牛血清白蛋白(BSA)/50 mol/L磷酸盐缓冲液(PBS), pH值7.4]封闭1 h, 甩干后立刻加入成膜液室温放置2 h, 甩干后除湿间干燥24 h左右, 抽真空封袋, 4 ℃保存。
3. 酶标抗体的制备 取CEA单克隆标记抗体2 mg与ALP 1 mg混合, 按戊二醛一步标记法进行标记, 分装后置-20 ℃保存。用酶标记物稀释液将酶标记物稀释至1 000倍, 以此浓度批量制备ALP酶标抗体, 4 ℃保存。
4. 发光强度(RLU)稳定性研究 用发光稀释液将化学发光剂分别以50、100和200倍稀释成8种不同浓度的化学发光底物液, 并在4~10 ℃、20~50 ℃和30~37 ℃时分别进行标准曲线检测实验, 确定为100倍稀释度和20~25 ℃为最佳实验条件, 30 min即可达到RLU的平台期, RLU稳定性也较好。
5. 校准品的制备 取经国家CEA标准品标定的CEA纯品, 用含0.5% BSA、pH值7.5的50 mmol/L PBS稀释至2、5、12、30、75和150 ng/mL, S0为稀释液, 分装为每瓶0.5 mL, -20 ℃保存。
6. 质控品的制备 采集经检测CEA含量< 5 ng/mL且乙型肝炎表面抗原(HBsAg)、乙型肝炎e抗原(HBeAg)和丙型肝炎病毒(HCV)抗体为阴性的正常人血清, 加入适量的CEA纯品及0.1%的高效防腐剂Proclin-300, 制成低、中、高质控血清, 然后经5次化学发光免疫实验由标准曲线求出浓度值, 分别计算他们的平均值为质控值。-16 ℃以下低温保存。
7. 测定方法的建立 本试剂盒采用双抗体夹心一步法, 即在包被微孔中加入CEA校准品或待测血清及酶标抗体各50 μ L, 用微量震荡器充分振荡混匀后, 置37 ℃温育反应。用洗涤液洗包被板5次, 每孔加入50 μ L化学发光底物液, 避光放置30 min后于发光分析仪上测量每孔的RLU值, 以校准品各点浓度的对数值为横坐标, 相对应的RLU值的对数值为纵坐标做标准曲线, 由标准曲线即可求出标本的浓度值。37 ℃温育60 min为较佳的实验条件, 可满足试剂盒所需的各项指标, 故确定反应条件为37 ℃温育60 min。
以稀释液进行10次重复测定, 其平均值加上2倍标准差求出对应的浓度值, 分别用不同批次的试剂和标准曲线进行3次实验, 求出平均浓度值作为本试剂盒的敏感性。经3次实验, 其敏感性为0.058 ng/mL。
用3份正常人血清配制成低、中、高质控血清, 在同一批实验中测定他们的RLU值, 每个质控血清平行做20孔, 批内精密度结果显示, 低值变异系数(CV)5.5%, 中值CV 6.7%, 高值CV 9.3%。
用3份正常人血清配制成低、中、高质控血清, 分别于不同实验日测定他们的浓度值, 共做20次, 他们的批间精密度结果显示, 低值CV 12.0%, 中值CV 10.3%, 高值CV 10.2%。本试剂盒的批间精密度CV< 15.0%。
1. 将30 ng/mL的CEA 5 mL分成5份, 每份1 mL, 每份加入1 mL的150 U/mL糖类抗原(CA) 199、1 mL的400 U/mL CA125、1 mL的60 ng/mL前列腺抗原(PSA)、1 mL的400 ng/mL甲胎蛋白(AFP)和1 mL的零标准(对照), 同时进行检测, 交叉反应率< 8.4%。
2. 将150 U/mL 的CA199、500 U/mL的CA125、120 ng/mL的PSA、400 ng/mL的AFP作为标本进行检测, 与他们的交叉反应率< 8.1%。
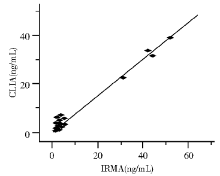
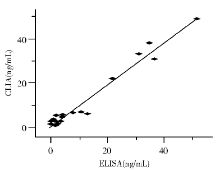
1. 取不同浓度的40份血清标本, 分别用CLIA、放射免疫分析法(IRMA)和ELISA同时测定CEA, 分别以北京科美东雅生物技术有限公司IRMA和ELISA CEA的测定值为X轴, 本法的测定值为Y轴, 结果经统计学处理, 相关系数(r)=0.991, Y=0.393 5+0.730 4X和r=0.984, Y=0.930 7+0.931 0X, 表明CLIA与IRMA和ELISA分别呈高度相关。见图1、2。
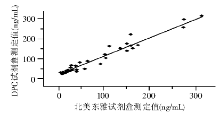
2. 70份血清标本, 分别用CLIA测定值作为X轴、德普公司(DPC)测定结果为Y轴, 经过统计学处理, r=0.979, Y=1.425 7+0.980 5X (70例), 表明2种试剂盒测定结果呈高度相关。见图3。
向正常混合血清中加入20、50、120、300和750 ng/mL不同浓度的CEA校准品, 测定其回收率为93.0%~106.0%, 平均为97.3%。
检测150份正常人血清标本, CEA含量为0.452~5.03 ng/mL, 平均为2.77 ng/mL。血清正常值可控制在5 ng/mL以下。
试剂盒放置37 ℃ 5 d后各项检测指标CV均< 4.70%, 表明试剂盒的稳定性良好。
取750 ng/mL浓度的CEA校准品, 分别以1/10、2/10、3/10、4/10、5/10、6/10、7/10、8/10、9/10、10/10倍比稀释值为X轴, 以实际测定值为Y轴, 在坐标轴上画图, 该曲线拐点即为该试剂盒的线性范围, 为0~250 ng/mL。
本研究采用ALP标记CEA单抗, 经过实验研究创建了戊二醛一步标记法, 该方法简便快速, 并能较好地保持酶和抗体的活性。
我们实验研究出的新型固相抗体包被技术, 使用一种双功能交联剂形成共价连接, 加上成膜工艺可使包被板高度均一, 并能长期保存(2年)。我们对该试剂盒的各项指标进行了检测, 其敏感性可达0.058 ng/mL; 精密性实验得到批内与批间CV分别为5.5%~9.3%和10.2%~12.2%, 表明方法的精密性较好, 可满足临床检测的要求; 特异性分析表明, 与CA199、CA125、PSA、AFP的交叉反应率均很小; 经实验表明, 本CLIA与IRMA和ELISA分别呈高度相关, r分别为0.991和0.984; 平均回收率为97.3%; 37 ℃稳定性实验结果说明试剂盒的稳定性良好。
实验结果表明, 我们研制的CEA CLIA试剂盒的各项指标均达到或超过了ELISA和IRMA。目前国内所用的CLIA试剂盒均为国外生产的封闭式全自动化学发光测量系统, 我们的检测系统为开放式操作, 简便快速, 不需要昂贵的全自动化学发光测量仪, 特别适合广大的中小医院推广使用, 为临床诊断和科研工作提供一种非常有价值的检测手段。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|