作者简介:刘 娟,女,1968年生,学士,副主任技师,主要从事免疫临床项目检测工作。
研究无症状乙型肝炎病毒(HBV)携带者中HBV表面抗原(HBsAg)含量与HBV复制的相关性。
方法采集HBV携带者血清152例,应用电化学发光法检测HBsAg含量[以标本吸光度值与仪器所给临界值(Cut-off)的比值勤(COI)表示]、酶联免疫吸附试验(ELISA)检测HBV e抗原(HBeAg)、聚合酶链反应(PCR)检测HBV DNA。按照HBV DNA检测结果将病例分为4组。Ⅰ组(54例)、Ⅱ组(34例)HBV DNA水平分别为<103拷贝/mL、103~105拷贝/mL,两组HBeAg皆为阴性;Ⅲ组(32例)HBV DNA水平为105~107拷贝/mL, 其中HBeAg阳性8例,阴性24例;Ⅳ组(32例)HBV DNA水平>107拷贝/mL,HBeAg皆为阳性。
结果HBsAg含量与HBV DNA水平呈显著对数相关( r=0.623, P<0.001)。各组平均Log HBsAg COI分别为Ⅰ组2.65±0.85,Ⅱ组2.95±0.76,Ⅲ组3.19±0.49,Ⅳ组4.65±0.37,其中Ⅳ组显著高于其他任何一组( P<0.001);Ⅰ组显著低于Ⅲ组( P=0.001)。根据受试者工作特征(ROC)曲线,Ⅳ组鉴别于其他各组的最佳分界值为HBsAgCOI=9 250(敏感性96.9%,特异性90.8%);而Ⅰ组鉴别于其他各组的最佳分界值为HBsAgCOI=1 250 (敏感性68.5%,特异性62.5%)。
结论HBsAg含量的检测在临床上判断HBV复制方面不失为一种即经济又简便的PCR替代方法。
乙型肝炎(简称乙肝)是由乙肝病毒(HBV)引起, 以肝脏炎症病变为主并可引起多器官损坏的一种传染病。我国人群中约有3%~5% HBV感染者血肝功能检测正常, 肝脏组织学基本正常, 无体征, 这类人群称为无症状HBV携带者。其中89%的HBV e抗原(HBeAg)阳性和17% HBV e抗体(抗-HBe)阳性的无症状HBV携带者体内存在高水平的HBV复制。这类人群发展为肝硬化、肝癌的风险远大于非病毒血症者[1]。因此, HBeAg阳性与否, 是否存在持续的病毒血症是评价HBV携带者预后的主要因素。众所周知, HBV DNA是评价HBV复制程度精确而重要的检测手段, 但因其操作复杂, 成本较高, 试验条件严格, 基层医院较难开展。早在1968年, Prince[2]指出HBV表面抗原(HBsAg)的检出是诊断HBV感染的最敏感而特异的指标。本研究采用电化学发光法对标本中HBsAg进行检测, 以标本吸光度与仪器所给临界值(Cut-off)的比值(COI)表示HBsAg含量, 并分析其与HBV DNA的相关性, 旨在研究其可否作为HBV复制的指标从而代替HBV DNA的检测并广泛应用于临床。
2004年11月至2006年3月来我院体检者, 从中筛选HBsAg阳性, 丙氨酸氨基转移酶(ALT)、天门冬氨酸氨基转移酶(AST)、胆红素正常且肝脏B超无异常者152例, 其中男96例, 女56例, 年龄28~52岁。采集血样, 分离血清冰冻保存并集中进行HBsAg、HBeAg及HBV DNA检测。
1.HBV DNA检测 采用荧光定量聚合酶链反应(PCR), 仪器为美国的ABI5700基因分析仪, 试剂由中山医科大学达安生物公司提供, 常规操作。
2.HBeAg检测 采用酶联免疫吸附试验(ELISA), 仪器为意大利ELISE全自动酶免疫分析仪, 试剂由上海荣盛公司提供, 按仪器和试剂说明书操作。
3.HBsAg检测 采用电化学发光法, 仪器为瑞士罗氏公司的2010电化学发光免疫分析仪, 试剂由瑞士罗氏公司提供, 按仪器说明书操作。
所有数据采用SPSS 11.0软件处理。各组HBsAg含量以LogHBsAgCOI表示, 多组间均值比较采用方差分析; 组间两两比较采用q检验。应用Pearon's相关及线性回归分析, 通过受试者工作特征(ROC)曲线图确定分界值。
一、根据HBV DNA测定结果将病例分为4组。HBV DNA含量分别为Ⅰ 组< 103拷贝/mL, Ⅱ 组103~105拷贝/mL, Ⅲ 组105~107拷贝/mL, Ⅳ 组> 107拷贝/mL。前2组HBeAg皆为阴性, Ⅲ 组中有8例HBeAg阳性, 24例HBeAg阴性。Ⅳ 组HBeAg皆为阳性。分别计算各组LogHBsAgCOI值 , Ⅰ 组2.65± 0.85, Ⅱ 组2.95± 0.76, Ⅲ 组3.19± 0.49, Ⅳ 组4.65± 0.37, 各组间差异有统计学意义(P< 0.001)。其中Ⅰ 组与Ⅲ 组比较差异有统计学意义(P=0.001), Ⅳ 与其他3组比较差异均有统计学意义(P< 0.001), 见表1。
| 表1 4组HBV DNA水平及各组LogHBsAgCOI值比较( |
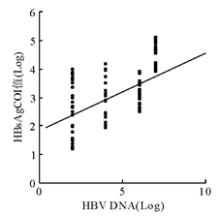
二、 HBV DNA含量与 HBsAgCOI值进行对数相关性分析, 为便于统计, 将4组LogHBV DNA约等于2、4、6、7, 得出r=0.623(P< 0.001), 表明HBV DNA含量与HBsAgCOI值呈对数相关。见图1。
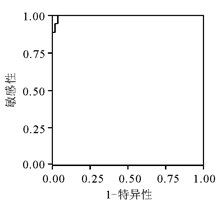
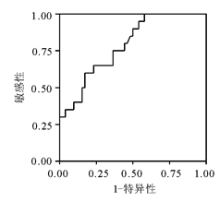
三、 通过ROC图, 确定Ⅳ 组区别于其他组的最佳分界值为HBsAgCOI=9 250(敏感性为96.9%, 特异性为90.8%); Ⅰ 组区别于其他组的最佳分界值为HBsAgCOI=1 250(敏感性为68.5%, 特异性为62.5%), 见图2~4。
尽管HBeAg阳性是HBV复制活跃和具有传染性的指标, 但近年研究发现, HBeAg阴性并不表明HBV 复制的终止或病毒血症的消失[3]。本研究中有66例HBV DNA水平在103~107拷贝/mL之间, 其中58例HBeAg为阴性。这可能是HBV基因组前C 区发生变异而导致HBeAg表达障碍所致[4], 说明以HBeAg判断机体是否存在HBV复制或病毒血症已不够科学。HBV DNA定量检测可反应HBV复制情况, 但在某些情况下, 当病毒DNA 与宿主肝细胞DNA整合到一起时, 会导致HBV DNA检测阴性。同时, 由于HBV DNA定量检测技术需要引物, 即便选择待测目的基因的保守区序列来设计引物, 也有一些突变频率较高的区域或位点, 导致在检测中出现假阴性[5]。而且HBV DNA定量检测技术对实验室条件要求比较严格, 在基层医院推广比较困难。HBsAg是HBV感染最早出现的标志物, HBsAg阳性标志着病毒的存在, 同时有病毒复制释放到血液中。本研究采用电化学发光检测技术对标本HBsAg进行检测, 结果显示HBsAg含量与HBV DNA水平呈显著对数相关, 从Ⅰ 组到Ⅳ 组, 随着HBV DNA水平的升高, HBsAg含量亦呈升高趋势, 说明HBsAg含量检测可以反应机体内病毒复制情况, 这与国外报道一致[6]。同时本研究通过绘制ROC曲线发现当HBsAgCOI> 9 250时, 预示机体病毒复制活跃, HBV DNA含量> 107拷贝/mL时, 其敏感性和特异性分别为96.9%和90.8%; 当HBsAg COI< 1 250时, 预示机体病毒复制抑制, HBV DNA含量< 103拷贝/mL时, 其敏感性和特异性分别为68.5%和62.5%。综上所述, 高HBsAg含量的无症状HBV携带者病毒复制还是很活跃的, 因此对于这种患者, 虽然ALT正常, 建议临床上应定期进行肝脏相应检查。
采用电化学发光检测技术检测HBsAg, 与传统的ELISA比较, 大大提高了检测的敏感性和特异性, 同时避免了前带现象。在没有条件开展PCR的实验室, 采用电化学发光技术检测 HBsAg可大致评价患者体内病毒复制情况, 从而指导临床用药或做进一步检查。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|