作者简介:朱岚,女,1979年生,学士,助理研究员,主要从事临床免疫分析研究。
目的建立甲状腺球蛋白抗体(TgAb)时间分辨荧光免疫分析(TRFIA)竞争检测法。方法 用甲状腺球蛋白抗原包被96孔板,用铕(Eu3+)标记羊抗鼠IgG做标记物,TRFIA检测人血清中的TgAb。结果 TgAb-TRFIA的敏感性为1.0 IU/mL;批内变异系数(
Objective To establish a time-resolved fluoroimmunoassay(TRFIA)for anti-thyroglobulin antibody(TgAb). Methods The thyroglobulin antigen was coated on the 96 well plates. A goat anti-mouse IgG-europium (Eu3+) was used to the detection. Serum TgAb level was detected by TRFIA. Results The sensitivity was 1.0 IU/mL. The within-run coefficient of variation (
甲状腺球蛋白抗体(anti-thyroglobulin antibody,TgAb) 是一种重要的抗甲状腺自身抗体,其异常增高常见于桥本病(Hashimoto′s disease,HD)等自身免疫性甲状腺疾病,然而临床上亦见于并不伴有HD 的甲状腺癌(thyroid cancer,TC)、甲状腺腺瘤(thyroid adenoma,TA)和结节性甲状腺肿(nodulargoiter,NG)等疾病[ 1, 2, 3]。目前市场上的TgAb定量试剂盒多由国外进口,采用酶联免疫吸附试验(ELISA)、化学发光法测定[ 4],经过探索和研究,本室创建了新型超敏感的TgAb时间分辨荧光免疫分析(time-resolved fluoroimmunoassay,TRFIA)检测法。
1. 标本 取自江苏省江原医院住院和门诊患者血清151例(患者均无心、肝、肺、肾等疾病,年龄27~68岁,平均年龄43.6岁)、正常体检人员血清252例(受检者年龄23~65岁,平均年龄39.7岁)。
2. 试剂和仪器 羊抗鼠IgG(华美生物工程公司产品);甲状腺球蛋白抗原、TgAb(Medix公司,鼠源);防腐剂(Proclin-300,SUPELCO公司)、聚氧乙烯山梨糖醇酐单月桂酸酯(Tween 20,Sigma公司);牛血清白蛋白(BSA,深圳晶美生物工程有限公司);铕(Eu3+)标记盒(PE公司);凝胶过滤柱(Sepharose CL-6B,Pharmacia公司)。TgAb国家标准品(150556-200601,中国药品生物制品检定所)。96孔微孔板(Nunc公司)。洗脱液、增强液、洗涤液、质控品均为自配,其他试剂均为国产分析纯。冻干机(上海东富龙冷冻干燥设备公司)。DELFIA1235全自动TRFIA检测仪(PE公司)。
1. TgAb标准品的配制 收集临床测定的TgAb高值血清,其乙型肝炎病毒抗原(HBV-Ag)、丙型肝炎病毒抗体(抗HCV)、人类免疫缺陷病毒抗体(抗HIV)均阴性,合并,加防腐剂(Proclin-300)适量。经反复冻融、离心、过滤等处理后得到标准品原液,用人去激素血清(含0.1%叠氮钠)配制成不同浓度的标准品,与用TgAb国家标准品配制成的已知浓度的校准品同时测量,校准各标准点的浓度,1 mL/瓶分装,冻干,–20 ℃保存[ 3]。
2. 固相抗原包被板的制备 甲状腺球蛋白抗原用50 mmol/L Na2CO3-NaHCO3 pH值9.6缓冲液稀释至合适浓度,200 μL/孔包被,振荡30 min,4 ℃过夜。弃包被液,每孔加250 μL 含有10% BSA的上述缓冲液封闭2 h,真空抽干,密封,置–20 ℃保存。
3. Eu3+-羊抗鼠IgG的制备 1 mg的羊抗鼠IgG加入含有1 mg的Eu3+-N2-[p-异氰酸-苄基]-二乙烯三胺四乙酸(Eu3+-DTTA)冻干粉的小瓶中,25 ℃磁力搅拌反应20 h。反应液经用80 mmol/L 三羟甲基氨基甲烷(Tris)-HCl pH值7.8缓冲液平衡的Sepharose CL-6B柱(1 cm×40 cm)层析,控制流速为2 mL/min,每管收集2 mL,吸光度( A)280监测收集第一蛋白峰。
4. 竞争TgAb-TRFIA检测方法 在包被甲状腺球蛋白抗原的微孔反应板中加入100 μL样本和100 μL用分析缓冲液稀释的TgAb,25 ℃振荡1 h,洗涤4次,再加入200 μL用分析缓冲液稀释的Eu3+-羊抗鼠IgG,25 ℃振荡0.5 h,洗涤4次,再加入增强液200 μL, 25 ℃振荡反应5 min后检测。该过程由DELFIA1235全自动TRFIA检测仪自动完成。
TgAb-TRFIA标准曲线分析[有效剂量(ED)、变异系数( CV)等]及结果由DELFIA全自动TRFIA检测仪随机配备的Multicalc软件自动给出。应用SPSS 12.0统计软件进行 t检验和相关回归分析, P<0.05为差异有统计学意义。
1. 固相甲状腺球蛋白抗原包被浓度 包被浓度分别为0.125、0.25、0.5、1.0、2.0、4.0、8.0 μg/mL,进行TgAb-TRFIA,结果显示2 μg/mL包被板时检测其零浓度点的结合率较高,曲线的斜率最大。所以选择甲状腺球蛋白抗原2 μg/mL浓度包板,达到获得良好免疫反应的条件。
2. 抗体稀释比例选择 在96孔微孔板中加入用分析缓冲液稀释的不同浓度的TgAb。结果表明,30%~50%抗体结合率对应的稀释度约为1∶2 000~1∶4 000倍。我们选择1∶2 000 倍抗血清稀释度为建立竞争抑制免疫分析的工作浓度。
1. TgAb-TRFIA标准品定值 以国家标准品为标准对照,定标品实际浓度与标示浓度回归方程为 Y=1 .013 2 X–0 .531 2( r=0 .999 9, P<0.05)。
2. TgAb-TRFIA标准曲线 采用Log/Log_B 数学拟合模式,以标准品含量对数值为横坐标,相应反应孔荧光计数(CPS)的对数值为纵坐标,绘制剂量-反应曲线,方法学线性范围为0~40 001.0 IU/mL。见 图1。
3. 敏感性 重复测定零剂量点(20次),以
4. 健全性 将TgAb浓度分别为298、584和3 562 IU/mL的3份血清进行倍比稀释,经测定稀释倍数与样本含量呈线性关系,相关系数分别为0.999 6、0.999 8、0.999 9;相关方程分别为 Y=298 .69 X–1 .92、 Y=587 .22 X+0 .30、 Y=3 568 .71 X+1 .17,表明本法具有良好的健全性。
5. 精密度 取本实验室自备的低、中、高浓度的TgAb质控冻干品各20份,批内、批间(20例)试验数据见 表1。
| 表1 批内、批间试验数据表(20例) |
6. 准确度 取含量为36.7 IU/mL的TgAb血清分别加到50、100、1 000 IU/mL标准参考品中进行回收试验。回收率分别为99.1%、97.3%、97.3%,平均回收率为97.9%。
7. 稳定性试验 将该试剂盒置于37 ℃ 7 d和4 ℃保存的整套试剂盒,双孔平行对比检测标准参考品,结果相关性良好( Y=0 .938 7 X–0 .971 7, r=0 .999 9, P<0 .05)。
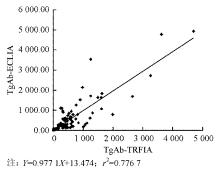
1. 比对试验 用TgAb-TRFIA与电化学发光分析技术(ECLIA)[ 4]平行测定175例样本(其中24例甲状腺功能正常、64例HD、45例Graves病、19例TC、23例NG),结果2种方法之间相关性良好( r=0 .881 3, P<0.05),见 图2。
2. 正常值范围 选择252例正常人血清样本,其甲状腺自身抗体阴性(包括TgAb),无甲状腺疾病史,未触及甲状腺肿,未服用除雌激素外的药物[ 4, 5]。结果显示男女TgAb平均值分别为107和110 IU/mL,差异无统计学意义( P>0.05),故合并为正常对照组,正常值取99%可信限,其参考值范围为≤110 IU/mL。
TRFIA是20世纪80年代发展起来的一种公认的最有发展前途的非放射免疫标记技术,具有敏感性高、特异性强、稳定性好、测定范围宽、操作简便等优点。本法的同类试剂盒有PE公司的TgAb-TRFIA试剂盒,但其采用的是间接法,由于正常血清中含高浓度的非特异性抗体,患者血清中受检的特异性IgG只占总IgG中的一小部分,而IgG的吸附性很强,非特异IgG可直接吸附到固相载体上,有时也可吸附到包被抗原的表面,在检测过程中样本须先行稀释(1∶40~1∶200),以避免过高的阴性本底影响结果的判断,但这种干扰因素还是有可能造成假阳性反应的,而且间接法成功的关键在于抗原的纯度,这就会使试剂盒的成本居高不下。
本法是基于微孔板免疫学竞争法的原理,用甲状腺球蛋白抗原包被板,在孔中加入标准参考品(或样本)及特异性的鼠源TgAb,同时竞争抗原的结合位点,再加入的Eu3+-羊抗鼠IgG可以结合到鼠源的TgAb上,形成抗原- TgAb-Eu3+标记羊抗鼠IgG的多层免疫复合物,加入增强液,微孔表面免疫复合物中的Eu3+被荧光增强液解离并形成稳定的荧光配合物,在TRFIA检测仪上测定相应发光强度。根据已知TgAb浓度的系列标准品的相应发光强度可得到标准曲线,未知样本的TgAb浓度可以通过其相应发光强度从曲线上反算出来,样本中的TgAb浓度与发光强度呈反比。
本法采用竞争原理测定TgAb,即样本中的抗体和一定量的TgAb共同竞争与固相抗原结合,再用Eu3+标二抗来示踪TgAb的量。这样就避免了间接法中的干扰因素,而且由于竞争法抗原的包被浓度降低,使成本降低;血清样本也不需要预稀释,减少临床操作工序,减轻工作强度。该法敏感性达1.0 IU/mL,精密度良好(批内 CV分别为3.3%~4.1%,批间 CV分别为3.7%~4.7%),平均回收率为97.9%,热稳定性好,与ECLIA比对,两法之间相关性良好( r=0.881 3),与临床结果的一致性好,该法成本不高,具有良好的应用价值[ 5, 6]。
样本采用静脉采血于凝血管中[可使用肝素,但不能使用乙二胺四乙酸(EDTA)或枸橼酸盐作抗凝剂],2~8 ℃条件下,样本可保存7 d,–20 ℃可长期保存,但要避免样本反复冻融。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|