作者简介:王青,男,1968年生,学士,副主任技师,主要从事临床血液与体液检验及实验室管理工作。
制备一种重复性好、稳定期长的尿有形成分质控品,有助于日常检验工作中对尿中有形成分进行质量控制。
方法按美国临床实验室标准化协会(CLSI)GP16-A3文件要求收集不同肾病患者的尿液,固定后分装保存。使用具备流式细胞术、显微摄影法和染色技术原理的设备,观察红细胞(RBC)、白细胞(WBC)、上皮细胞、管型和细菌存在与否和形态保持情况;按CLSI EP25文件要求观察各类有形成分的稳定性;同时配制高、中、低3种不同浓度质控品进行精密度检测。
结果有形成分质控品中所含RBC、WBC、上皮细胞、管型和细菌等有形成分的形态保持良好,易于辨认。重复性较好,RBC变异系数(
制备的尿有形成分质控品含有RBC、WBC、上皮细胞、管型和细菌等有形成分,且有较好的重复性和稳定性,适用于临床尿有形成分质控之用途。
To prepare a quality control material of urinary formed elements with good repeatability and stability, and improve the quality control of urinary formed elements in the routine urine test.
MethodsAccording to Clinical and Laboratory Standards Institute (CLSI) GP16-A3,a variety of urine samples from the kidney disease patients was collected, stabilized and stored. By means of flow cytometry, microscopy and staining technique, the existence and storage state of red blood cells (RBC),whit blood cells (WBC), epithelial cell, casts and bacteria were observed in terms of CLSI EP25 requirement. Meanwhile,the control materials with high, medium and low concentrations were prepared to measure precision.
ResultsThe quality control material of urinary formed elements presented good holdings and easily identified feature of RBC,WBC,epithelial cell,casts and bacteria. The results of coefficient of variation (
The prepared quality control material of urinary formed elements contains RBC,WBC,epithelial cell,casts and bacteria. It shows relatively good repeatability and stability,and can be used for quality control of urine test in clinical laboratory.
尿有形成分检验的质量控制是一个比较困难的问题。美国临床实验室标准化协会(CLSI)GP16-A3指出,尿有形成分的质量控制应采用商品化质控品每日进行。我国《尿液沉渣检查标准化的建议》及推广全自动尿液沉渣分析仪的目的,旨在减少方法和技术差异导致的检验结果误差,合适的质控物已成为提高实验室检验可靠性的关键。目前,国外已有商品化的尿有形成分质控品,但仅包含红细胞(RBC)、白细胞(WBC)2种有形成分。而按GP16-A3的要求所能监测的有形成分太少,用于日常尿有形成分分析的质控有一定的困难。因此,我们试图研制出一种含各种有形成分的尿有形成分质控品,并能将其方法逐步推广应用于临床检测实验室。
1、 尿液样本 取自上海仁济医院不同肾脏疾病住院患者。
2、 试剂与仪器 离心机、甲醛(美国Sigma公司);UF-500、UF-1000尿液有形成分分析仪 (简称UF-500、UF-1000,日本Sysmex公司);IQ 200尿液有形成分分析仪(简称IQ 200,美国IRIS公司);Combi XS全自动尿有形成分分析仪(简称Combi XS,德国科宝公司);FUS100尿沉渣影像工作站(简称FUS100,长春迪瑞医疗科技有限公司);显微摄影装置(日本Olympus公司)。
1、按常规方法收集不同肾脏疾病患者尿液,离心取沉淀。用中性甲醛溶液按适当的比例进行固定。将已固定的尿液有形成分混匀后,加盖标记后放入2~8 ℃冰箱保存。
2、用不同仪器进行检测,截取UF-500、UF-1000的直方图和IQ 200、Combi XS、FUS100及显微摄影的照片。设置不同监测点在UF-500上监测,观察其稳定性。
3、用生理盐水或正常人尿液将其中的RBC、WBC、上皮细胞和管型分别配制成高、中、低(医学决定水平)3种不同的浓度,在UF-500上作重复检测,观察其不精密度。
一、自制的这种产品包含RBC、WBC、上皮细胞和管型等有形成分,适用于UF系列仪器、IQ200、Combi XS和FUS100等尿有形成分分析仪,见 图1~6。
二、自制尿有形成分质控品中RBC、WBC、上皮细胞和管型的高、中、低3种浓度在UF-500上检测的不精密度分别为RBC 18~586个/μL, CV 4.4%~7.8%;WBC 17~128个/ μL, CV 4.3%~14.3%;上皮细胞 6~60个/μL, CV 4.8%~14.4%;管型3~9个/μL, CV 16.9%~23.3%,见 表1。
| 表1 UF-500检测的4种主要参数高、中、低3种浓度的不精密度 |
三、自制尿有形成分质控品不同参数随时间变化情况见 图7~10。用SPSS13.0回归拟合曲线分析结果见 表2。
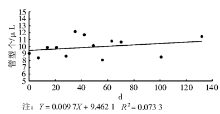 | 图10 管型稳定性监测 |
| 表2 不同参数监测值SPSS13.0回归拟合曲线分析结果 |
尿液检查因取材方便,通过对尿理化检查可观察尿一般性状和化学成分,通过对尿中有形成分如RBC、WBC、上皮细胞、管型、结晶、吞噬细胞、肿瘤细胞、细菌、精子等观察,可识别尿中病理改变,对泌尿系统及其相关疾病具有诊断、疗效观察和预后判断的价值。随着尿液分析仪作为尿液分析的过筛手段[ 1~ 3],尤其是尿干化学试带分析仪,因其简便、快速、重复性好、一次检测可以报告多个分析参数等优点[ 4],已被临床实验室广泛应用。但尿液有形成分检查仍然需要显微镜人工检测,其方法费时费力,不同检验人员间差异较大。为了保证尿液检查质量,CLSI专门发布文件[ 5]指导尿液样本收集、运送、保存和分析,我国血液、体液专家委员会也提出《尿液有形成分检验标准化的建议》,为我国尿液有形成分检查标准化提供指导。同时,为了减少检验人员尿液有形成分镜检的负荷、改善检验流程、减少人为因素引起的误差、推动尿有形成分检查的标准化,自动化有形成分分析仪相继问世[ 1~ 3, 6~ 9]。然而,尿液有形成分质控仍缺乏好的质控品,日本Sysmex公司使用不同直径大小的微粒子作为质控物,美国IRIS公司、长春迪瑞公司使用固定人RBC作为质控物,美国伯乐公司的尿质控品中有形成分也仅含RBC、WBC,这些质控品的问题有的是微粒子而非细胞成分,只好用于计数而不能用于形态观察;有的所含成分偏少,只有RBC或RBC、WBC,不能对尿液有形成分分析仪的主要检测参数进行有效监控;还有些市售的尿液有形成分分析仪根本就没有质控品,其分析的质量令人担忧。为了改善这种情况,保证尿有形成分检查的质量,我们探索和尝试尿有形成分分析质控品的制备工作,以期对尿液有形成分分析仪的运行状况进行有效的监控。
从 图1~6可以看出自制的尿有形成分质控品在不同检测原理的尿液有形成分分析仪,抑或是相差显微镜中,均检出了RBC、WBC、上皮细胞、管型、细菌等有形成分,说明制备的尿有形成分质量控制品中包含了RBC、WBC、上皮细胞、管型、细菌等有形成分,能满足日常尿液有形成分分析仪对上述尿液成分的监控,可用于不同检测原理的有形成分分析仪,也适用于尿有形成分显微镜检查的质量控制。
从 表1可以看出本研究制备的尿有形成分质量控制品不同参数不同浓度的天内不精密度( CV)分别为RBC 7.78%(18.39/μL)、5.89%(44.18/μL)和4.38%(586.98/μL);WBC 14.24%(16.62/μL)、4.93%(32.62/μL)和4.33%(127.78/μL);上皮细胞14.38%(8.67/μL)、9.80%(19.72 /μL)和4.76%(60.15/ μL);管型23.25%(2.88/μL)、19.37%(4.46/μL)和16.97%(8.44/μL)。与BEN-EZRA等[ 10]用新鲜尿样本做批内精密度的结果基本一致(RBC 2.4%~31.0%;WBC 8.5%~14.0%;上皮细胞7.0%~18.0%;管型17.0%~45.0%),与Sutheesophon等[ 11]所做的批内精密度也相一致(RBC 2.93%~16.28%;WBC 2.07%~22.31%;上皮细胞6.18%~11.36%;管型12.38%~35.00%),说明本研究制备的尿有形成分质控品与新鲜尿样本和微粒子质控品具有相似的批内精密度,既保持了尿液的天然属性,又具有与粒子计数相当的不精密度,至少可满足流式细胞术加核酸荧光染色技术之尿有形成分分析仪质控的需要。至于制备的尿有形成分质控品在其他检测原理的分析仪上的精度测定,因所制质控品不多,尚需在下一阶段继续做完。
从 表2和 图7~10可见本研究制备的尿有形成分质控品中RBC、WBC、上皮细胞和管型在监测日内没有随时间而发生趋向性变化,斜率差异无统计学意义[ 12]( P>0.05)。由此说明这几个项目是稳定的,稳定期至少为130 d,有关稳定性的进一步研究和监测仍在进行中。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|










